
| A. | 可溶于水 | B. | 水溶液能导电 | C. | 熔融状态可导电 | D. | 熔点350℃ |
分析 某种化合物中一定存在离子键,说明该化合物中是离子化合物,离子化合物在熔融状态下能导电,共价化合物在熔融状态下不能导电,据此分析解答.
解答 解:某种化合物中一定存在离子键,说明该化合物中是离子化合物,离子化合物在熔融状态下能导电,共价化合物在熔融状态下不能导电,
A.可溶于水的化合物可能是共价化合物,如HCl,故A错误;
B.水溶液能导电的化合物可能是共价化合物,如二氧化硫等,故B错误;
C.熔融状态下可导电的化合物中含有自由移动的阴阳离子,所以该化合物的构成微粒是阴阳离子,为离子化合物,一定含有离子键,故C正确;
D.熔点350℃可能是共价化合物,故D错误;
故选C.
点评 本题考查离子化合物的判断,侧重考查基本概念,明确离子化合物和共价化合物的根本区别是解本题关键,注意不能根据溶解性、电解质溶液酸碱性及导电能力强弱判断离子化合物,为易错点.


科目:高中化学 来源: 题型:解答题

| 推测 | 操作和现象 | 结论 |
| 杂质中的正盐成分可能有: Na2S Na2CO3 Na2SO3 Na2SO4 | ①取Wg产品配成稀溶液; ②向溶液中滴加过量BaCl2溶液,有白色沉淀生成,过滤,得沉淀和滤液; ③向沉淀中加入过量盐酸,沉淀完全溶解,并有刺激性气味的气体产生. ④向滤液滴加2滴淀粉溶液,再逐滴加0.100 0mol•L-1碘的标准溶液,至溶液呈紫色不再褪去,消耗碘的标准溶液体积为18.10mL. | 产品杂质中: 一定含有Na2SO3, 可能含有Na2S、Na2CO3, 一定不含有Na2SO4. 操作④发生的反应是: 2S2O${\;}_{3}^{2-}$+I2═S4O${\;}_{6}^{2-}$+2I- 产品纯度:$\frac{9}{w}$×100%. |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
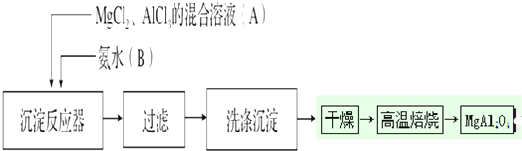
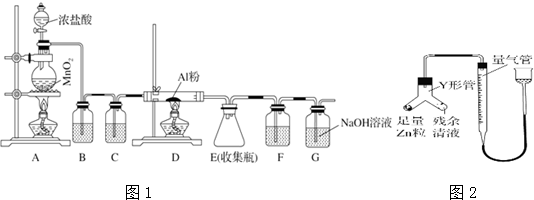
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢气通过灼热的CuO粉末 | B. | 碳与SiO2高温反应制粗硅 | ||
| C. | 将锌粒投入Cu(NO3)2溶液 | D. | 镁条在CO2中燃烧 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,11.2L的甲烷气体含有甲烷分子数为0.5 NA | |
| B. | 14g乙烯和丙烯的混合物中总原子数为3 NA | |
| C. | 标准状况下,22.4 L氯仿中含有的氯原子数目为3 NA | |
| D. | 17.6 g丙烷中所含的极性共价键为4 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
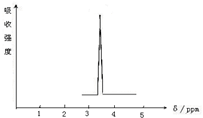 利用核磁共振技术测定有机物分子的三维结构的研究获得了2002年诺贝尔化学奖.
利用核磁共振技术测定有机物分子的三维结构的研究获得了2002年诺贝尔化学奖.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 灼热的炭与二氧化碳反应 | |
| B. | 铁和稀硫酸的反应 | |
| C. | 氢氧化钡晶体的粉末和氯化铵晶体混合 | |
| D. | 生石灰溶于水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com