
科目:高中化学 来源:不详 题型:单选题
| A.用米汤检验加碘盐中的碘酸钾(KIO3) |
| B.用食用醋除去热水瓶中积存的水垢 |
| C.用纯碱(Na2CO3)溶液洗涤沾有油污的器具 |
| D.用灼烧并闻气味的方法区分化纤织物与纯毛织物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.将氢氧化钠固体放在滤纸上称量 |
| B.用10ml量筒量取8.58ml蒸馏水 |
| C.制取氯气时,用二氧化锰与浓盐酸在常温下反应,并用排水集气法收集 |
| D.配制氯化铁溶液时,将一定量氯化铁溶解在较浓的盐酸中,再用水稀释到所需浓度 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 编号 | 实验内容 | 实验目的 |
| A | 将SO2通入酸性KMnO4溶液中 | 证明SO2具有漂白性 |
| B | 将F2通入NaBr溶液中 | 比较氟与溴的氧化性强弱 |
| C | 将铜与浓硝酸反应生成的气体收集后用冰水混合物冷却降温 | 研究温度对化学平衡的影响 |
| D | 分别向2支试管中加入相同体积不同浓度的H2O2溶液,再向其中1支加入少量MnO2 | 研究催化剂对H2O2分解速率的影响 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
| 稀硫酸用量 | 剩余固体质量 |
| 第一次加入10g | mg |
| 第二次加入10g | 2.0g |
| 第三次加入10g | 1.5g |
| 第四次加入10g | 1.0g |
| 第五次加入10g | 0.6g |
| 第六次加入10g | 0.6g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
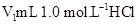 溶液和
溶液和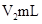 未知浓度的NaOH溶液混合均匀后,测量并记录溶液温度,所得实验结果如右下图所示(实验中始终保持
未知浓度的NaOH溶液混合均匀后,测量并记录溶液温度,所得实验结果如右下图所示(实验中始终保持 )。
)。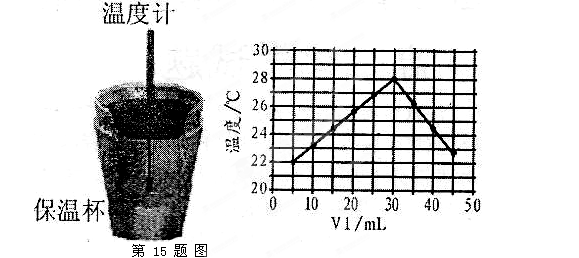 (1)从实验装置上看,左图中尚缺少的一种玻璃用品是________________________。
(1)从实验装置上看,左图中尚缺少的一种玻璃用品是________________________。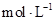
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
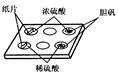
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
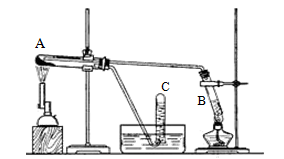
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com