
| A、金刚石的网状结构中,由共价键形成的最小碳环上有6个碳原子 | B、白磷分子晶体中,微粒之间通过共价键结合,键角为60° | C、在NaCl晶体中每个Na+(或C1-)周围都紧邻6个Cl-(或Na+) | D、离子晶体在熔化时,离于键被破坏,而分子晶体熔化时,化学键不被破坏 |


 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案科目:高中化学 来源: 题型:
| A、在SiO2晶体中,每个Si原子与4个O原子形成共价键 | B、在面心立方密堆积的金属晶体中,每个金属原子周围紧邻的有4个金属原子 | C、NaCl晶体中与每个Na+距离相等且最近的Cl-有6个 | D、CsCl晶体中与每个Cs+距离相等且最近的Cl-有8个 |
查看答案和解析>>
科目:高中化学 来源: 题型:
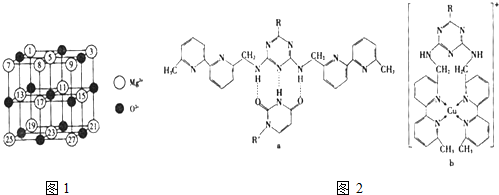
| 氟化物 | NaF | MgF2 | SiF4 |
| 熔点/K | 1266 | 1534 | 183 |
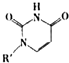 或Cu(I)(I表示化合价为+1)时,分别形成a和b:
或Cu(I)(I表示化合价为+1)时,分别形成a和b:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com