
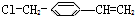 推测它不可能具有下列哪种性质( )
推测它不可能具有下列哪种性质( )| A. | 能被酸性高锰酸钾溶液氧化 | B. | 能使溴水发生加成反应而褪色 | ||
| C. | 能发生水解反应 | D. | 易溶于水,也易溶于有机溶剂 |
分析 该分子中含有氯原子、碳碳双键和苯环,具有氯代烃、烯烃、苯的性质,能发生取代反应、水解反应、氧化反应、加成反应、还原反应、加聚反应,据此分析解答.
解答 解:A.含有碳碳双键,所以能被酸性高锰酸钾溶液氧化生成-COOH,故A不选;
B.含有碳碳双键,所以能和溴发生加成反应而使溴水褪色,故B不选;
C.含有氯原子,能发生水解反应生成-CH2OH,故C不选;
D.不含亲水基,只含憎水基,所以不易溶于水,根据相似相溶原理知,易溶于有机溶剂,故D选;
故选D.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系即可解答,侧重考查卤代烃、烯烃性质,注意:即使不含碳碳双键,如果苯环上连接-CH2CH3也能被酸性高锰酸钾溶液氧化,题目难度不大.


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:解答题
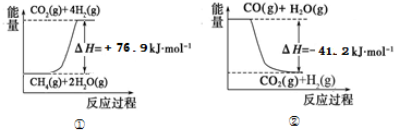
 | 15.2MPa | 20.3MPa | 30.4MPa |
| 400℃ | 32.8% | 38.8% | 48.2% |
| 450℃ | 22.4% | 27.5% | 35.9% |
| 500℃ | 14.9% | 18.8% | 25.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol的氢氧根离子所含电子数均为9 NA | |
| B. | 1.00 mol NaCl中含有NA个NaCl分子 | |
| C. | 常温常压下,92g的NO2和N2O4的混合气体含有的原子数为6NA | |
| D. | 常温常压下,22.4L氯气与足量铁粉充分反应,转移的电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素 | N | S | O | Si |
| 原子半径/10-10m | 0.75 | 1.02 | 0.74 | 1.17 |
| A. | 0.80×10-10m | B. | 0.70×10-10m | C. | 1.20×10-10m | D. | 1.10×10-10m |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将相同大小、形状的镁条和铝条与相同浓度的盐酸反应时,两者速率一样大 | |
| B. | 将浓硝酸分别放在冷暗处和强光照射下,会发现光照可以加快浓硝酸的分解 | |
| C. | 在相同条件下,等质量的大理石块和大理石粉与相同的盐酸反应,大理石粉反应快 | |
| D. | 两支试管中分别加入相同质量的氯酸钾,其中一支试管中再加入少量二氧化锰,同时加热,产生氧气的快慢不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
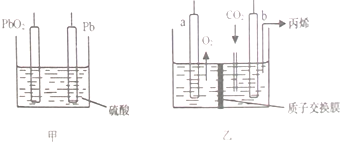
| A. | 为实现工作原理,PbO2电极应与b电极相连 | |
| B. | b电极反应式为:3CO2+18e-+18H+=6H2O+CH3CH=CH2 | |
| C. | 在铅蓄电池供电过程中,Pb电极质量不断减小 | |
| D. | 乙装置中H+由b电极向a电极移动 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com