
【题目】等物质的量的下列烃完全燃烧,消耗氧气最多的是( )
A.C6H6
B.C2H6
C.C3H6
D.CH4
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某学校化学学习小组为探究二氧化氮的性质,按下图所示装置进行实验。

请回答下列问题:
(1)装置甲中盛放浓硝酸的仪器A的名称是__________,该装置中发生反应的化学方程式为_________________________。
(2)实验过程中,装置乙、丙中出现的现象分别是:____________________、____________________;装置丙中的试管内发生反应的离子方程式为:_____________________。
(3)取下装置丙中的试管D,在其中滴加FeSO4溶液,溶液变为__________色,为了证明铁元素在该反应中的产物可以____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】全钒液流电池,简称钒电池,它的电能是以化学能的方式存储在不同价态钒离子的硫酸电解液中,采用质子交换膜作为电池组的隔膜,电解质溶液平行流过电极表面并发生电化学反应。电池总反应为VO2++V3++H2O![]() V2++VO2++2H+。下图是钒电池基本工作原理示意图。下列说法错误的是
V2++VO2++2H+。下图是钒电池基本工作原理示意图。下列说法错误的是

A. 电池完全放电后,正、负极分别为VO2+和V3+离子溶液
B. 放电时,负极反应式为V2+-e-=V3+
C. 充电过程中,负极电解液的pH不变
D. 充电时,阳极反应式为VO2++H2O-e-=VO2++2H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钠在供氧、防腐、除臭、微量分析等多方面有着重要用途,工业生产过氧化钠的方法是将除去二氧化碳且干燥后的空气通入熔融的钠(温度180~200℃)中得到氧化钠,然后增加空气流量并迅速升高温度至300~400℃即可得到过氧化钠。某化学兴趣小组模拟工业流程制备过氧化钠的装置如图所示。

请回答下列相关问题。
(1)浓硫酸的作用是______________。
(2)升温至300~400℃时发生主要反应的化学方程式是______________。
(3)下列选项中的加热方式适合该实验的是_____(填字母)。
A.水浴 B.油裕(100~260℃) C.控温电炉(150~500℃) D.酒精喷灯(1000~1200℃)
(4)若要提高产品纯度,需在具支试管后添加一个装置,该装置应该是________。
(5)在具支试管后添加(4)中所要求的装置后,某同学还认为制得的过氧化钠中还含有少量的某种杂质,该杂质是________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示500℃时,X、Y、Z三种气体在容积固定的容器中反应,各物质的浓度随时间的变化情况.达到平衡后,改变压强,平衡不移动.下列说法中正确的是( ) 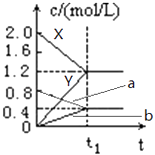
A.Z物质的变化情况为曲线b
B.该反应的化学方程式为:2X(g)3Y(g)+Z(g)
C.0→t1 , X的物质的量浓度变化量为1.2mol/L
D.若t1=1min,则v(Y )=0.02molL﹣1s﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用化学原理可以对工厂排放的废水、废渣等进行有效检测和处理.某工厂对制铬工业污泥中Cr(Ⅲ)的回收与再利用工艺如下(硫酸浸液中金属离子主要是Cr3+ , 其次是Fe3+、Fe2+、Al3+、Ca2+、Mg2+): 
常温下部分阳离子的氢氧化物形成沉淀时溶液的pH见下表:
阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Ca2+ | Cr3+ |
开始沉淀时的pH | 1.9 | 7.0 | 9.6 | 4.2 | 9.7 | |
沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8.0 | 11.7 | 9.0(>9.0 溶解) |
(1)酸浸时,为了提高浸取率可采取的措施是(至少一条).
(2)调pH=4.0是为了除去
(3)钠离子交换树脂的作用原理为Mn++nNaR→MRn+nNa+ , 被交换的杂质离子是
(4)试配平下列氧化还原反应方程式:Fe2++H2O2+H+═Fe3++
(5)通入SO2的目的是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com