
| A. | 用镊子夹取钠块,吸干表面的煤油后,用小刀切下一部分进行实验.剩余的钠应放回原试剂瓶 | |
| B. | 钠加热后先熔化成小球状,这是因为金属钠的熔点较低 | |
| C. | 钠燃烧时火焰呈黄色,这与钠元素的焰色反应有关 | |
| D. | 钠块表面若有部分已被氧化为Na2O,充分燃烧后将得到Na2O和Na2O2的混合物 |
分析 A.钠易与空气中氧气和水反应,应保存在煤油中;
B.依据钠的熔点低的物理性质解答;
C.焰色反应为元素的物理性质;
D.氧化钠不稳定,受热易生成过氧化钠.
解答 解:A.做金属钠的性质实验时,剩余的钠放回原试剂瓶,由于钠很活泼,且如果将钠随意丢弃容易引起火灾、爆炸等事故,故A正确;
B.金属钠的熔点较低,钠加热后先熔化成小球状,故B正确;
C.焰色反应为元素的物理性质,钠燃烧时火焰呈黄色,故C正确;
D.氧化钠不稳定,受热易生成过氧化钠,所以钠块表面若有部分已被氧化为Na2O,充分燃烧后将得到Na2O2,故D错误;
故选:D.
点评 本题考查了钠的性质,熟悉钠的物理性质和化学性质是解题关键,注意焰色反应为元素性质,题目难度不大.


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:选择题
| A. | HCl(aq)+NaOH(aq)═NaCl(aq)+H2O(l) | B. | 2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l) | ||
| C. | 4Fe(OH)2(s)+2H2O(l)+O2(g)═4Fe(OH)3(s) | D. | 2H2(g)+O2(g)═2H2O(l) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两者均为弱酸 | |
| B. | 两者均可使紫色石蕊试液变红色 | |
| C. | CO2气体通入Na2SiO3溶液中可以制得硅酸 | |
| D. | 两者受热时均可以分解 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+═2Fe(OH)3+3Mg2+ | |
| B. | 粗铜精炼时,与电源负极相连的是纯铜,电极反应式为:Cu2++2e-═Cu | |
| C. | 用Pt电极电解氯化铝溶液:2Cl-+2 H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2+2OH- | |
| D. | 由Mg、Al、NaOH溶液组成原电池,其负极反应式为:Al-3e-+4OH-═AlO2-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
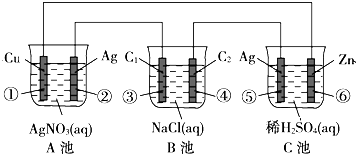
| A. | ①②④⑦ | B. | ①②④⑤ | C. | ②③④⑤ | D. | ①②⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1gH2和4gO2反应放出71.45kJ热量,则氢气的燃烧热为142.9 kJ•mol-1 | |
| B. | 在稀溶液中,H+(aq)+OH-(aq)═H2O(1)△H=-57.3 kJ•mol-1,若将含0.5molH2SO4的浓硫酸与含1molNaOH的氢氧化钠溶液混合,放出的热量大于57.3kJ | |
| C. | HCl和NaOH反应的中和热△H=-57.3 kJ•mol-1,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ•mol-1 | |
| D. | 1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷燃烧热 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去).A$\stackrel{O_{2}}{→}$B$\stackrel{O_{2}}{→}$C
A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去).A$\stackrel{O_{2}}{→}$B$\stackrel{O_{2}}{→}$C查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com