
| A. | 新制氯水放置数天,溶液中的Cl2分子数目不变 | |
| B. | 久置的氯水可使蓝色石蕊试纸先变红后褪色 | |
| C. | 钠长时间露置于空气中,最终得到Na2CO3粉末 | |
| D. | 钠投入硫酸铜溶液中有红色粉末产生 |
分析 A.新制氯水放置数天,HClO分解,促进氯气与水的反应正向移动;
B.久置的氯水中只含盐酸;
C.Na很活泼,在空气中能够发生一系列反应;
D.钠投入硫酸铜溶液中,Na先与水反应生成NaOH和氢气,再发生NaOH与硫酸铜的复分解反应.
解答 解:A.新制氯水放置数天,HClO分解,促进氯气与水的反应正向移动,则溶液中的Cl2分子数目减少,故A错误;
B.久置的氯水中只含盐酸,则使蓝色石蕊试纸变红,不会褪色,故B错误;
C.单质钠长久露置在空气中最终产物为Na2CO3,其转化过程为:Na→Na2O→NaOH→Na2CO3•10H2O→Na2CO3,故C正确;
D.钠投入硫酸铜溶液中,Na先与水反应生成NaOH和氢气,再发生NaOH与硫酸铜的复分解反应生成蓝色沉淀,不会生成Cu,故D错误;
故选C.
点评 本题考查物质的性质及氧化还原反应,为高频考点,把握发生的氧化还原反应为解答的关键,注意物质的性质、发生的反应判断、平衡移动及氯水的成分等知识点即可解答,综合性较强,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | SO2、NO、SiO2都是酸性氧化物 | |
| B. | PM2.5是指大气中直径接近于2.5xl0 -6m的颗粒物,它在空气中形成气溶胶 | |
| C. | 向蛋白质溶液中滴加CuS04溶液产生沉淀属于化学变化 | |
| D. | KCl和SO3溶于水后均能导电,是因为KC1和S03都为电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可用氧化物形式表示为BaO•CuO•2SiO2 | |
| B. | 性质稳定,不易脱色 | |
| C. | 易溶解于强酸和强碱 | |
| D. | x等于6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
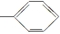 ⑤-CHO ⑥-H.
⑤-CHO ⑥-H.| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L水中含有1molH2SO4 | B. | 1L溶液中含有1molH+ | ||
| C. | 1LH2SO4溶液中含98g H2SO4 | D. | 将98g H2SO4溶于1L水配成溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molH2质量为2g | B. | H2O的摩尔质量为18g | ||
| C. | 标况下44g CO2的体积为22.4L | D. | 9.8g H2SO4含1mol的H2SO4分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 一定含有Al,其质量为4.5g | |
| B. | 一定含有(NH4)2SO4和MgCl2,且物质的量相等 | |
| C. | 一定含有MgCl2和FeCl2 | |
| D. | 一定不含FeCl2,可能含有MgCl2和AlCl3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
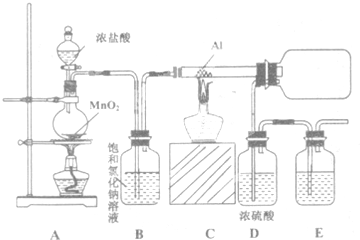
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com