
某烃结构式如下: -C≡C-CH=CH-CH3,有关其结构说法正确的是
-C≡C-CH=CH-CH3,有关其结构说法正确的是
A.所有原子可能在同一平面上 B.所有原子可能在同一条直线上
C.所有碳原子可能在同一平面上 D.所有氢原子可能在同一平面上
科目:高中化学 来源:2016届四川省邛崃市高三强化训练一化学试卷(解析版) 题型:选择题
在一定温度下,将等量的气体分别通入起始体积相同的密闭容器Ⅰ和Ⅱ中,使其发生反应,t0时容器Ⅰ中达到化学平衡,X、Y、Z的物质的量的变化如图所示。则下列有关推断正确的是( )

A.该反应的化学方程式为:3X+2Y 2Z
2Z
B.若两容器中均达到平衡时,两容器的体积V(Ⅰ)<V(Ⅱ),则容器Ⅱ达到平衡所需时间小于t0
C.若两容器中均达到平衡时,两容器中Z的物质的量分数相同,则Y为固态或液态
D.若达平衡后,对容器Ⅱ升高温度时,其体积增大,说明Z发生的反应为吸热反应
查看答案和解析>>
科目:高中化学 来源:2016届宁夏银川市高三4月质检理综化学试卷(解析版) 题型:实验题
钛被称为“二十一世纪金属”,工业上用钛铁矿制备金属钛的工艺流程如下:
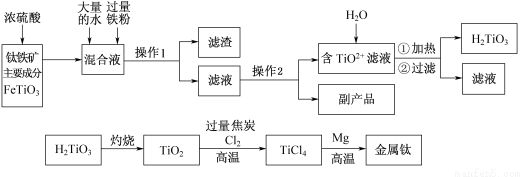
已知:钛铁矿主要成分与浓硫酸反应的主要产物是TiOSO4和FeSO4,TiOSO4遇水会水解。
请回答下列问题:
(1)操作1用到的玻璃仪器除烧杯外还有 ,操作2是 、过滤,副产品主要成分的化学式为 。
(2)请结合化学用语解释将TiO2+转化为H2TiO3的原理 。
(3)已知钛的还原性介于铝与锌之间,估计钛能耐腐蚀的原因之一是 。如果可从Na、Zn、Fe三种金属中选一种金属代替流程中的镁,那么该金属跟四氯化钛反应的化学方程式是 。
(4)电解TiO2来获得Ti是以TiO2作阴极,石墨为阳极,熔融CaO为电解质,用碳块作电解槽,其阴极反应的电极反应式是 。
(5)为测定溶液中TiOSO4的含量,首先取待测钛液10 mL用水稀释至100 mL,加过量铝粉,充分振荡,使其完全反应:3TiO2+ +Al+6H+=3Ti3++Al3++3H2O。过滤后,取出滤液20.00 mL,向其中滴加2~3滴KSCN溶液作指示剂,用 (填一种玻璃仪器的名称)滴加0.1000mol·L-1 FeCl3溶液,发生Ti3++Fe3+=Ti4++Fe2+。当溶液出现红色达到滴定终点,用去了30.00mL FeC13溶液。待测钛液中TiOSO4的物质的量浓度是 。
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三5月模拟一理综化学试卷(解析版) 题型:选择题
下列有关电解质溶液中粒子浓度关系正确的是
A.pH=a的醋酸溶液,稀释10倍后,其pH=b,则a=b-1
B.含等物质的量的NaHSO3和Na2SO3的溶液:2c(Na+)=3[c(HSO3-)+c(SO32-)+c(H2SO3)]
C.0.1mol·L-1盐酸与0.2mol·L-1氨水等体积混合:c(NH3·H2O)>c(Cl-)>c(NH4+)>c(OH-)
D.含有AgCl和AgI固体的悬浊液:c(Ag+)>c(Cl-)=c(I-)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年海南嘉积中学高二下期中理科化学试卷(解析版) 题型:填空题
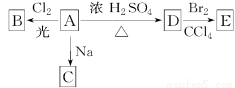
(1)化合物A(C4H10O)是一种有机溶剂。A可以发生以下变化:
①A分子中的官能团名称是____________;
②A只有一种一氯取代物B,写出A的结构简式:____________;
③A的同分异构体F也可以有框图内A的各种变化,且F的一氯取代物有三种,F的结构简式是
______________________________________。
(2)化合物“HQ”(C6H6O2)可用作显影剂,“HQ”可以与三氯化铁溶液发生显色反应。“HQ”还能发生的反应是(选填序号)____________________。
①加成反应 ②氧化反应 ③加聚反应 ④水解反应[
“HQ”的一硝基取代物只有一种。“HQ”的结构简式是______________________。
(3)A与“HQ”在一定条件下相互作用形成水与一种食品抗氧化剂“TBHQ”。“TBHQ”与氢氧化钠溶液作用得到分子式为C10H12O2Na2的化合物。“TBHQ”的结构简式是____________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年海南嘉积中学高二下期中理科化学试卷(解析版) 题型:选择题
下列有机物在核磁共振氢谱上只给出一组峰的是
A .HCHO B .CH3OH C.HCOOH D.CH3COOCH3
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三下学期考前练习化学试卷(解析版) 题型:填空题
【物质结构与性质】
原子序数小于36的X、Y、Z和铜四种元素,X的基态原子有3个不同的能级,有一个能级中的电子数比其它两个能级中的电子数都多1;Y基态原子中的电子占有5个轨道,其中有2个轨道处于半充满状态,Z的原子序数为24。
(1)Z原子基态核外电子排布式为______________________________;
(2)元素X与Y的第一电离能较大的是_________(填元素符号);H2Y2中Y原子轨道的杂化类型为____;
(3)+3价Z的配合物K[Z(C2O4)2(H2O)2]中的配体是_________;与C2O42-互为等电子体的一种分子的化学式为_____________;
(4)Cu和Y形成的化合物的晶胞如图所示,晶胞中与铜离子距离相等且最近的铜离子有_______个.某种有缺陷的铜和Y形成的化合物的晶体由Cu2+、Cu3+、Y2-及空隙组成,可表示为Cu0.98Y,则n(Cu2+)/n(Cu3+)=_______________。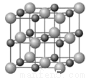
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三下学期考前练习化学试卷(解析版) 题型:选择题
工业上常利用铝粉和氧化铁反应来焊接铁轨。下列说法正确的是
A.氧化铝、氧化铁均为两性氧化物
B.氧化铝中的微粒半径:r(Al3+)>r(O2-)
C.在该反应中,铝的还原性强于铁的还原性
D.1mol 氧化铁参加反应转移电子数约为4×6.02×1023
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川成都石室中学高二4月月考化学试卷(解析版) 题型:选择题
设N A为阿伏加德罗常数的值,下列叙述正确的是
A.60gSiO 2晶体有σ键4N A
B.在标准状况下,2.24 LSO3中含有的氧原子数为0.3NA
C.t℃时,MgCO3的 Ksp=4×10-6,则饱和溶液中含 Mg2+数目为2×10-3NA
D.标准状况下,2.24LCl2通入足量H2O溶液中转移的电子数为0.1NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com