
【题目】“宏观-微观-符号”是学习化学的重要内容和方法。下列有关说法错误的是( )

A.甲乙容器中所给物质的组成微粒均为分子
B.甲乙容器可以得出结论为:凡是化学反应,反应前后分子总数不会发生变化
C.此反应后碳元素的化合价升高
D.图甲所示物质中碳、氢元素的质量比是3:1
科目:高中化学 来源: 题型:
【题目】海水淡化是解决沿海城市饮用水问题的关键技术。下图是电渗析法淡化海水装置的工作原理示意图(电解槽内部的“┆”和“│”表示不同类型的离子交换膜)。工作过程中b电极上持续产生Cl2。下列关于该装置的说法错误的是
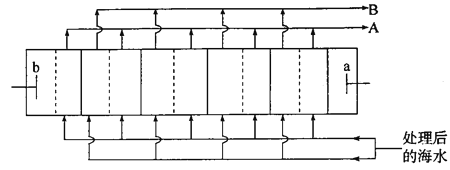
A. 工作过程中b极电势高于a极
B. “┆”表示阴离子交换膜,“│”表示阳离子交换膜
C. 海水预处理主要是除去Ca2+、Mg2+等
D. A口流出的是“浓水”,B口流出的是淡水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二茂铁在常温下为橙黄色粉末,有樟脑气味,用作节能、消烟、助燃添加剂等。可用下列方法合成:
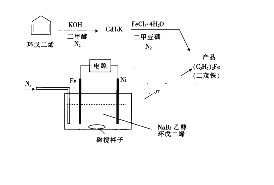
回答下列问题:
(1)室温下,环戊二烯以二聚体的形式存在。某实验小组要得到环戊二烯,需先将环戊二烯二聚体解聚,已知:
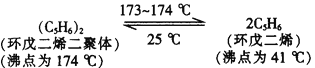
①分离得到环戊二烯的操作为_____________________(填操作名称)。
②由环戊二烯生成C5H5K的化学方程式为___________________。
(2)流程中所需的FeCl2·4H2O可通过下列步骤制得。
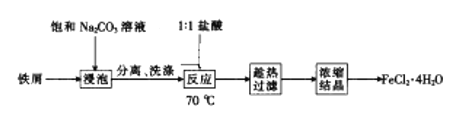
①用饱和Na2CO3溶液“浸泡”铁屑的目的是_____________________________________。
②采用“趁热过滤”,其原因是________________________________________________。
(3)用电解法制备二茂铁时:
①不断通入N2的目的是__________________________。
②Ni电极与电源的____________(填“正极”或“负极”)相连,电解过程中阳极的电极反应式为__________________,理论上电路中每转移1 mol电子,得到产品的质量为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯甲酸甲酯是一种重要的工业原料,某研究性学习小组的同学拟用下列装置制取高纯度的苯甲酸甲酯。

有关数据如下表:

请回答下列问题:
(1)在烧瓶中混合有机物及浓硫酸的方法是__;在实际实验中,甲醇、苯甲酸的物质的量之比远大于其理论上的物质的量之比,目的是__;装置C中除甲醇、苯甲酸与浓硫酸外还需要放置__。
(2)C装置上部的冷凝管的主要作用是__。
(3)制备和提纯苯甲酸甲酯的操作的先后顺序为(填装置字母代号)__。
(4)A装置锥形瓶中Na2CO3的作用是__;D装置的作用是__;当B装置中温度计显示__℃时可收集苯甲酸甲酯。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】薄荷油中含有少量的α—非兰烃和β—非兰烃,两者互为同分异构体,其相对分子质量为136。根据如下化学转化,回答相关问题:

已知: +R’CO2H
+R’CO2H
 +CO2
+CO2
(1)分别写出C→D和D→E的反应类型:___;___。
(2)写出B、F、H、β—非兰烃的结构简式:B:___;F:___;H:___;β—非兰烃:___。
(3)A的同分异构体中含有两个—COOCH3基团的化合物共有___种(不考虑手性异构),其中核磁共振氢谱呈现2个吸收峰的异构体结构简式为___。
(4)α—非兰烃与等物质的量的Br2进行加成反应的产物共有___种(不考虑立体异构)。
(5)写出C→M反应的化学方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学计量在化学中占有重要地位,根据相关计算填空:
①3gHe是________ molHe,含有的质子数为_______个。
②1.204×1023个NH3含________mol氨分子,在标准状况下的体积为________L。
③29.4克硫酸中含有原子总数为________ mol,与_______克NH3含有相同数目的氢原子。
④在标准状况下,1.6g某气态氧化物RO2体积为0.56L,该气体的物质的量是________ ,摩尔质量是________ ,R的相对原子量为________ 。
⑤已知Wg气体A含有a个分子,那么在标准状况下,bg气体A所占的体积是________ (其中阿伏加德罗常数用NA表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用右图所示装置进行下列实验,能得出相应实验结论的是( )
选项 | ① | ② | ③ | 实验结论 | 实验装置 |
A | 稀硫酸 | Na2S | AgNO3与AgCl的溶液 | Ksp(AgCl)>Ksp(Ag2S) |
|
B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 | |
C | 稀盐酸 | Na2SO3 | Ba(NO3)2 溶液 | SO2与可溶性钡盐均可以生成白色沉淀 | |
D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 酸性:硝酸>碳酸>硅酸 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环之间共用一个碳原子的化合物称为螺环化合物,螺[2,2]戊烷(![]() )是最简单的一种。下列关于该化合物的说法错误的是
)是最简单的一种。下列关于该化合物的说法错误的是
A. 与环戊烯互为同分异构体
B. 二氯代物超过两种
C. 所有碳原子均处同一平面
D. 生成1 molC5H12至少需要2 molH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用含砷氧化铜矿[含CuO、Cu2(OH)2CO3、As2O3及重金属盐等]制取Cu2(OH)2SO4的工艺流程如下:
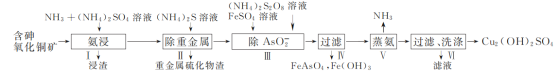
(1) 步骤Ⅰ“氨浸”时,控制温度为50~55 ℃,pH约为9.5,含铜化合物转化为[Cu(NH3)4]SO4溶液。
① CuO被浸取的离子方程式为________。
②浸取温度不宜超过55 ℃,其原因是________。
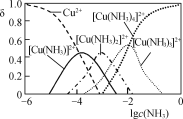
③ Cu2+与NH3结合时,溶液中含铜微粒的物质的量分布分数(δ)与溶液中游离的c(NH3)的对数值的关系如图所示。若用1 L浸取液(由等物质的量NH3和NH4+组成)将amolCu2(OH)2CO3全部浸出为[Cu(NH3)4]2+(CO32-转变为HCO3-,不考虑其他反应,溶液体积变化忽略不计),原浸取液中起始时c(NH3)应满足的条件是________。
(2) “除AsO2-”时,FeSO4需过量,一方面使AsO2-沉淀完全,另一目的是________。
(3) “蒸氨”时发生反应的化学方程式为________。
(4) 为了实现生产过程中物质循环利用,可采取的措施为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com