
【题目】烃A是一种重要的化工原料。已知A在标准状况下的密度为1.25 g·L-1,B可发生银镜反应。它们之间的转化关系如图:
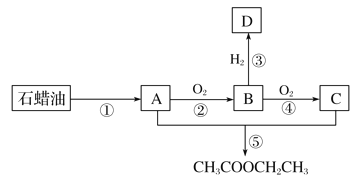
请回答:
(1)有机物B中含有的官能团名称是_______________________________________________。
(2)第⑤步发生加成反应,该反应的化学方程式是_________________________________。
(3)将金属钠与有机物D反应所得的少量产物溶于水,滴加2滴酚酞溶液,水溶液显红色,其原因是__________________(用化学方程式表示)。
(4)下列说法正确的是________。
A.有机物A与D在一定条件下可反应生成乙醚[(CH3CH2)2O]
B.用新制碱性氢氧化铜悬浊液无法区分有机物B、C和D
C.通过直接蒸馏乙酸乙酯和有机物C的混合物,可分离得到纯的乙酸乙酯
D.相同条件下乙酸乙酯在氢氧化钠溶液中水解较在稀硫酸中更完全
【答案】 醛基 CH2===CH2+CH3COOH![]() CH3COOCH2CH3 CH3CH2ONa+H2O―→CH3CH2OH+NaOH AD
CH3COOCH2CH3 CH3CH2ONa+H2O―→CH3CH2OH+NaOH AD
【解析】烃A在标准状况下的密度为1.25 g·L-1,A的摩尔质量为:1.25 g·L-1×22.4 L·mol-1=28 g·mol-1,则烃A为CH2=CH2;B可发生银镜反应,结合流程,则B为CH3CHO;C为CH3COOH;D为CH3CH2OH。
(1)B为CH3CHO,含有的官能团名称是醛基;(2)第⑤步发生加成反应,根据原子守恒,该反应的化学方程式是CH2=CH2+CH3COOH![]() CH3COOCH2CH3;(3)金属钠与乙醇反应生成乙醇钠,因为乙醇分子很难电离出H+,所以乙氧基离子(CH3CH2O-)有很大的夺走氢离子变成乙醇分子的倾向,所以乙醇钠溶液显碱性,用化学方程式表示为:CH3CH2ONa+H2O→CH3CH2OH+NaOH;(4)CH2=CH2有碳碳双键,一定条件可与CH3CH2OH发生加成反应,生成乙醚,A正确;新制碱性氢氧化铜悬浊液与乙醛加热可反应产生砖红色Cu2O,与乙酸发生中和反应,与乙醇不反应,故可用新制碱性氢氧化铜悬浊液区分上述三种物质,B错误;直接蒸馏乙酸乙酯和乙酸的混合物,会使乙酸乙酯中混入乙酸,可用先加入饱和碳酸钠溶液再分液的方法,C错误;D项,乙酸与氢氧化钠溶液中和反应,使乙酸乙酯在氢氧化钠溶液中水解较在稀硫酸中更完全,D正确;综上,选AD。
CH3COOCH2CH3;(3)金属钠与乙醇反应生成乙醇钠,因为乙醇分子很难电离出H+,所以乙氧基离子(CH3CH2O-)有很大的夺走氢离子变成乙醇分子的倾向,所以乙醇钠溶液显碱性,用化学方程式表示为:CH3CH2ONa+H2O→CH3CH2OH+NaOH;(4)CH2=CH2有碳碳双键,一定条件可与CH3CH2OH发生加成反应,生成乙醚,A正确;新制碱性氢氧化铜悬浊液与乙醛加热可反应产生砖红色Cu2O,与乙酸发生中和反应,与乙醇不反应,故可用新制碱性氢氧化铜悬浊液区分上述三种物质,B错误;直接蒸馏乙酸乙酯和乙酸的混合物,会使乙酸乙酯中混入乙酸,可用先加入饱和碳酸钠溶液再分液的方法,C错误;D项,乙酸与氢氧化钠溶液中和反应,使乙酸乙酯在氢氧化钠溶液中水解较在稀硫酸中更完全,D正确;综上,选AD。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】请根据下列有关规定的情景填空。
(1)①下图是除去氧化膜的镁条投入稀盐酸中产生氢气的速率随时间的变化关系,曲线前段出现高峰的主要影响因素是________。
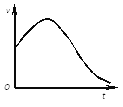
②下图是过氧化氢在酶的催化作用下分解速率随温度的变化关系,曲线后段明显下降的主要影响因素是__。
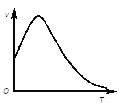
(2)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2。紫外光照射时,在不同催化剂(I、II、III)作用下,CH4产量随光照时间的变化见图。在0~15小时内,CH4的平均生成速率I、II和III从大到小的顺序为_________(填序号)。
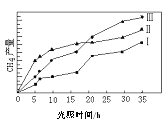
(3)以TiO2/Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率的关系见图。
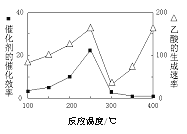
①250~300℃时,温度升高而乙酸的生成速率降低的原因是_____________。
②当温度的取值范围在________时,温度是影响乙酸的生成速率的主要因素。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列曲线中,纵坐标表示生成Al(OH)3的质量,横坐标表示加入试剂的体积。下列叙述中不正确的是( )
A. 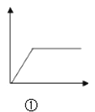 图①可表示向NH3·H2O中滴加AlCl3溶液至过量
图①可表示向NH3·H2O中滴加AlCl3溶液至过量
B. 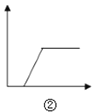 图②可表示向NaOH与NaAlO2的混合溶液中通入CO2至过量
图②可表示向NaOH与NaAlO2的混合溶液中通入CO2至过量
C. 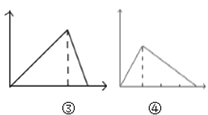 图③可表示向NaOH与NaAlO2的混合液中滴加HCl溶液至过量;而图④可表示向盐酸酸化的AlCl3溶液中滴加NaOH至过量
图③可表示向NaOH与NaAlO2的混合液中滴加HCl溶液至过量;而图④可表示向盐酸酸化的AlCl3溶液中滴加NaOH至过量
D. 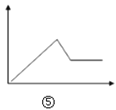 图⑤可表示向MgCl2和AlCl3的混合液中滴加NaOH溶液至过量
图⑤可表示向MgCl2和AlCl3的混合液中滴加NaOH溶液至过量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食品包装袋中有一个小纸袋,上面写着“石灰干燥剂”。
(1)“石灰干燥剂”的主要成分石灰是______________(填化学式),石灰所属的物质类型__________________(填序号)。
①金属氧化物 ②碱性氧化物 ③碱 ④碱性干燥剂 ⑤纯净物 ⑥化合物 ⑦盐
(2)生石灰可做干燥剂的理由是________________________(用化学方程式表示)。
(3)你认为下列内容还必须在这种小纸袋上注明的是____________(填序号)。
①禁止食用 ②可以食用 ③禁止未成年人用手拿 ④生产日期
(4)小纸袋中的物质能否长期地作干燥剂?为什么?_______________________________。
(5)某同学将浓硫酸、氢氧化钠固体、生石灰等物质划分为一类。该同学的分类依据为____________(填字母)。
A. 酸类 B. 碱类 C. 氧化物 D. 干燥剂
(6)生石灰还可以跟哪些类别的物质发生化学反应?请列举三例并填表。__________________、__________________、__________________、__________________、__________________、__________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据能量变化示意图,下列热化学方程式正确的是( )
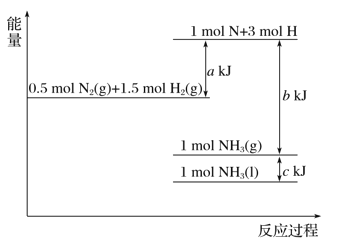
A. N2(g)+3H2(g)===2NH3(g) ΔH=-(b-a) kJ·mol-1
B. N2(g)+3H2(g)===2NH3(g) ΔH=-(a-b) kJ·mol-1
C. 2NH3(l)===N2(g)+3H2(g) ΔH=2(a+b-c) kJ·mol-1
D. 2NH3(l)===N2(g)+3H2(g) ΔH=2(b+c-a) kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食盐是日常生活的必需品,也是重要的化工原料。
(1)粗食盐中常含有少量K+、Ca2+、Mg2+、Fe3+、SO42-等杂质离子,实验室提纯NaCl的流程如下:

提供的试剂:饱和Na2CO3溶液 饱和K2CO3溶液 NaOH溶液 BaCl2溶液 Ba(NO3)2溶液 75%乙醇 四氯化碳
①欲除去溶液Ⅰ中的Ca2+、Mg2+、Fe3+、SO42-,选出a所代表的试剂,按滴加顺序依次为________(只填化学式)。
②分离操作①中所用到的玻璃仪器有____________。
③洗涤除去NaCl晶体表面附带的少量KCl,选用的试剂为________。
(2)用提纯的NaCl配制450 mL 4.00 mol·L-1NaCl溶液,所用仪器除药匙、烧杯、玻璃棒外还有________(填仪器名称)。
(3)在实验中多次用到玻璃棒,其作用有三个,分别是______________、______________、______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为确定Na2CO3和NaHCO3混合物样品的组成,称取四份该样品溶于水后分别逐滴加入相同浓度盐酸30.0 mL,充分反应,产生CO2的体积(已折算成标准状况下的体积,不考虑CO2在水中的溶解)如下表:
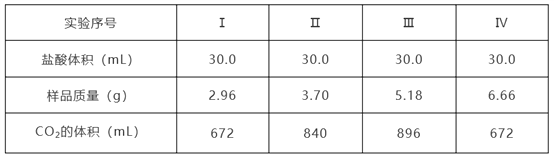
(1)样品中物质的量之比n(Na2CO3):n(NaHCO3)=_________。
(2)盐酸的物质的量浓度c(HCl)=______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组利用图甲装置制取氨气并探究氨气的有关性质。

(1)装置A中烧瓶内试剂可选用__(填序号)。
a.碱石灰 b.浓硫酸 c.五氧化二磷 d.氯化钙
(2)若探究氨气的溶解性,当装置D中集满氨气后,关闭K1、K2,打开K3,引发喷泉的实验操作是__。不能在K2的导管末端连接图乙中的__装置(填序号)。
(3)若探究氨气的还原性,需关闭K1、K3,K2连接纯净、干燥氯气的装置。
①用二氧化锰与浓盐酸制取氯气,生成的气体必须依次通过盛有__试剂和__试剂的洗气瓶。
②D中氨气与氯气反应产生白烟,同时生成一种无色无味的气体,该反应的化学方程式为__。
③尾气可用C装置处理,若尾气中含有少量Cl2,则C装置中应盛放__溶液(填化学式),反应的离子方程式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】373K时,某 1L密闭容器中加入2mol NH3发生如下可逆反应:2NH3(g)![]() N2(g)+3H2(g)。其中物质H2的物质的量变化如下图所示。
N2(g)+3H2(g)。其中物质H2的物质的量变化如下图所示。
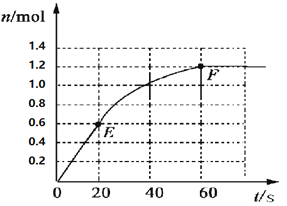
(1)前20 s内NH3(g)的平均反应速率为___________;
(2)373K时该反应的平衡常数的值为______________;
(3)若在此平衡体系中再加入1mol的NH3,与原平衡比较,新平衡时NH3的转化率______(填“增大”或“减小”,下同),NH3的平衡浓度_________。
(4)将原平衡升温至473K,重新达平衡时(其他条件不变),H2的平衡浓度为NH3的2倍,该反应的正反应为_________(填“放热反应”或“吸热反应”),为增大平衡体系中H2的物质的量,下列措施正确的是(其它条件相同)______。
a.升高温度 b.扩大容器的体积 c.加入合适的催化剂 d.再充入N2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com