
【题目】Na2CO3溶液中存在水解平衡:CO32-+H2O![]() HCO3-+OH-。下列说法错误的是( )
HCO3-+OH-。下列说法错误的是( )
A.加水稀释,溶液中所有离子的浓度都减小B.通入CO2,溶液pH减小
C.加入NaOH固体,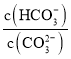 减小D.升高温度,平衡常数增大
减小D.升高温度,平衡常数增大
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】X、Y、Z、W四种短周期元素在周期表中的位置关系如右图所示,X原子最外层有5个电子。下列说法正确的是
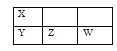
A.离子半径:W< Z2B.还原性:Z2<W
C.酸性:H3YO4 >HXO3D.氢化物的稳定性:YH3> H2Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A+B→C △H <0,分两步进行 ① A+B→X △H>0 ② X→C △H<0 。下列示意图中,能正确表示总反应过程中能量变化的是
A.  B.
B. 
C.  D.
D. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学以废旧铝制易拉罐为原料制备Al(OH)3其流程如图:
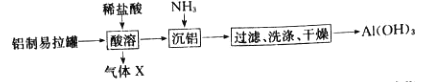
(1)“酸溶”时,增大盐酸的浓度反应速率将___(填“增大”或“减小”)。
(2)气体X是___(填“H2”或“CO2”)。
(3)一定条件下,将1molN2和3molH2置于lL密闭容器中合成NH3,10min后测得H2为l.2mol,则用H2表示该反应的速率为___molL-1min-1。
(4)氢氧化铝是___(从性质上分类)氢氧化物,它与盐酸反应的化学方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】迄今为止,煤不但是人类使用的主要能源,也是重要的化工原料。如图是以煤为原料合成聚苯乙烯塑料的流程。
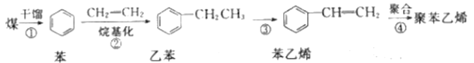
(1)苯在一定条件与Cl2反应可生成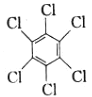 ,该反应类型为___(填“取代”或“加成”)反应;
,该反应类型为___(填“取代”或“加成”)反应;
(2)如图流程中原子利用率为100%的反应是___(填字母);
A.①③ B.②④
(3)能使酸性高锰酸钾溶液褪色的是___(填“![]() ”或“
”或“![]() ”)。
”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将等物质的量的A和B,混合于2 L的密闭容器中,发生如下反应:3A(g)+B(g) ![]() xC(g)+2D(g),5 min后测得c(D)=0.5 mol/L,c(A):c(B)=1:2,C的反应速率是0.15 mol/(L·min)。
xC(g)+2D(g),5 min后测得c(D)=0.5 mol/L,c(A):c(B)=1:2,C的反应速率是0.15 mol/(L·min)。
(1)B的反应速率v(B)=___,x=___。
(2)A在5 min末的浓度是_______。
(3)此时容器内的压强与开始时之比为:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电化学脱硫技术是一种温和的净化技术,其基本原理为利用阳极反应产生的羟基自由基(·OH,氧元素为-1价)将燃煤中的含硫物质氧化除去,其装置示意图如图所示。
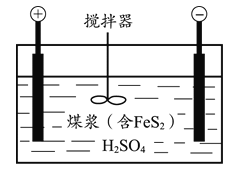
(1)将煤打成煤浆加入电解槽的目的是________。
(2)阳极的电极反应式为________。
(3)补全用羟基自由基除去煤中二硫化亚铁(FeS2)的反应的离子方程式:FeS2 +·OH =Fe3+ + SO42- + H2O +___。
(4)利用上述装置对某含FeS2的煤样品进行电解脱硫,测得一定时间内随溶液起始pH的改变脱硫率(溶于水中的硫元素质量占煤样中硫元素总质量的百分比)的变化如下图所示。

pH大于1.5后脱硫率下降的可能原因有:随着pH的升高,反应物的氧化性或还原性降低;________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应mA(固)+nB(气)![]() pC(气)+qD(气),反应过程中其它条件不变时C的百分含量C%与温度(T)和压强(P)的关系如图所示,下列叙述中正确的是
pC(气)+qD(气),反应过程中其它条件不变时C的百分含量C%与温度(T)和压强(P)的关系如图所示,下列叙述中正确的是
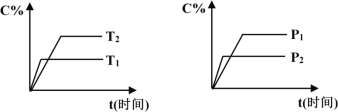
A. 达到平衡后,使用催化剂,C%将增大
B. 达到平衡后,若升高温度、化学平衡向逆反应方向移动
C. 方程式中n>p+q
D. 达到平衡后,增加A的量有利于化学平衡向正反应方向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com