
ΓΨΧβΡΩΓΩAΓΔBΓΔCΓΔD «ΥΡ÷÷≥ΘΦϊΒΡ”–ΜζΈοΘ§Τδ÷–AΒΡ≤ζΝΩΆ®≥Θ”Οά¥ΚβΝΩ“ΜΗωΙζΦ“ΒΡ ·”ΆΜ·ΙΛΖΔ’ΙΥ°ΤΫΘ§B”κC‘Ύ≈®ΝρΥαΚΆΦ”»»ΧθΦΰœ¬ΖΔ…ζΖ¥”ΠΘ§…ζ≥…ΒΡ”–ΜζΈο”–ΧΊ βœψΈΕΘΜAΓΔBΓΔCΓΔD‘Ύ“ΜΕ®ΧθΦΰœ¬ΒΡΉΣΜ·ΙΊœΒ»γΆΦΥυ ΨΘ®Ζ¥”ΠΧθΦΰ“― Γ¬‘Θ©ΘΚ
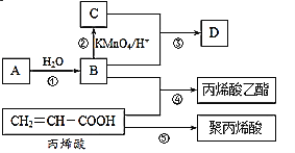
Θ®1Θ©C÷–ΙΌΡήΆ≈ΒΡΟϊ≥ΤΈΣ___Θ§ΔέΒΡΜ·―ßΖΫ≥Χ ΫΈΣ__ΓΘ
Θ®2Θ©±ϊœ©ΥαΘ®CH2=CHΘ≠COOHΘ©ΒΡ–‘÷ Ω…Ρή”–___ΓΘΘ®Εύ―ΓΘ©
AΘ°Φ”≥…Ζ¥”Π BΘ°»Γ¥ζΖ¥”Π CΘ°÷–ΚΆΖ¥”Π DΘ°―θΜ·Ζ¥”Π
Θ®3Θ©”Ο“Μ÷÷ΖΫΖ®Φχ±πBΚΆCΘ§Υυ”Ο ‘ΦΝ «__ΓΘ
Θ®4Θ©±ϊœ©Υα““θΞΒΡΫαΙΙΦρ ΫΈΣ___ΓΘ
ΓΨ¥πΑΗΓΩτ»Μυ CH3COOHΘΪCH3CH2OH![]() CH3COOC2H5ΘΪH2O ABCD ΧΦΥαΡΤ»ή“ΚΜρ’ΏΧΦΥα«βΡΤ»ή“ΚΜρΉœ…Ϊ ·»οΒ» CH2=CHCOOCH2CH3
CH3COOC2H5ΘΪH2O ABCD ΧΦΥαΡΤ»ή“ΚΜρ’ΏΧΦΥα«βΡΤ»ή“ΚΜρΉœ…Ϊ ·»οΒ» CH2=CHCOOCH2CH3
ΓΨΫβΈωΓΩ
ΗυΨίΧβΡΩ–≈œΔΩ…÷ΣA «““œ©Θ§““œ©Υ°Μ·ΒΟΒΫ““¥ΦΘ§BΈΣ““¥ΦΘ§““¥Φ±Μ―θΜ·ΚσΒΟΒΫ““ΥαΘ§“ρ¥ΥC «““ΥαΘ§D «Εΰ’ΏΖΔ…ζθΞΜ·Ζ¥”ΠΚσΒΟΒΫΒΡ““Υα““θΞΓΘ
Θ®1Θ©““ΥαΒΡΙΌΡήΆ≈ΈΣτ»ΜυΘ§Δέ «θΞΜ·Ζ¥”ΠΘ§ΖΫ≥Χ ΫΈΣCH3COOHΘΪCH3CH2OH![]() CH3COOC2H5ΘΪH2OΘΜ
CH3COOC2H5ΘΪH2OΘΜ
Θ®2Θ©ΧΦΧΦΥΪΦϋΩ…“‘ΖΔ…ζΦ”≥…Ζ¥”ΠΚΆ―θΜ·Ζ¥”ΠΘ§τ»ΜυΩ…“‘ΖΔ…ζ÷–ΚΆΖ¥”ΠΘ§ΕχΧΰ…œΒΡ«β‘≠Ή”Ω…“‘±Μ»Γ¥ζΘ§“ρ¥Υ¥πΑΗ―ΓABCDΘΜ
Θ®3Θ©““¥ΦΈόΥα–‘Θ§Εχ““Υα”–Υα–‘Θ§Ω…“‘”ΟΧΦΥαΡΤ»ή“ΚΓΔ ·»ο ‘“ΚΒ»ΖΫΖ®ά¥Φχ±πΘΜ
Θ®4Θ©±ϊœ©Υα““θΞΦ¥±ϊœ©ΥαΚΆ““¥Φ–Έ≥…ΒΡθΞΘ§ΤδΫαΙΙΈΣCH2=CHCOOCH2CH3ΓΘ



| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΡ≥―ß…ζΈΣ≤βΕ®Έ¥÷Σ≈®Ε»ΒΡΝρΥα»ή“ΚΘ§ Β―ι»γœ¬ΘΚ”Ο1.00 mL¥ΐ≤βΝρΥα≈δ÷Τ100 mLœΓΝρΥαΓΘ“‘0.12 molΓΛLΘ≠1ΒΡNaOH»ή“ΚΒΈΕ®…œ ωœΓH2SO4 25.00 mLΘ§ΒΈΕ®÷’÷Ι ±œϊΚΡNaOH»ή“Κ15.00 mLΓΘΗΟ―ß…ζ”Ο±ξΉΦ0.12 molΓΛLΘ≠1 NaOH»ή“ΚΒΈΕ®ΝρΥαΒΡ Β―ι≤ΌΉς»γœ¬ΘΚ
A.”Ο’τΝσΥ°œ¥Η…ΨΜΦν ΫΒΈΕ®ΙήΘΜ
B.Φλ≤ιΦν ΫΒΈΕ®Ιή «Ζώ¬©“ΚΘΜ
C.”Ο“Τ“ΚΙή»ΓœΓH2SO4 25.00 mLΘ§ΉΔ»κΉΕ–ΈΤΩ÷–Θ§Φ”»κ÷Η ΨΦΝΘΜ
D.ΫΪ±ξΉΦ“ΚΉΔ»κΦν ΫΒΈΕ®ΙήΩΧΕ»ΓΑ0Γ±“‘…œ2Θ≠3cm¥ΠΘ§‘ΌΑ―Φν ΫΒΈΕ®ΙήΙΧΕ®ΚΟΘ§ΒςΫΎ“ΚΟφ÷ΝΩΧΕ»ΓΑ0Γ±ΜρΓΑ0Γ±ΩΧΕ»“‘œ¬Θ§≤ΔΦ«¬ΦΕΝ ΐΘΜ
E.”Ο±ξΉΦΒΡNaOH»ή“Κ»σœ¥Φν ΫΒΈΕ®ΙήΘΜ
F.Α¥…œ ω≤ΌΉς÷ΊΗ¥ΝΫ÷Ν»ΐ¥ΈΘΜ
G.Α―ΉΕ–ΈΤΩΖ≈‘ΎΒΈΕ®Ιήœ¬ΟφΘ§ΤΩœ¬Βφ“Μ’≈ΑΉ÷ΫΘ§±ΏΒΈ±Ώ“ΓΕ·ΉΕ–ΈΤΩ÷±÷ΝΒΈΕ®÷’ΒψΘ§Φ«œ¬ΒΈΕ®Ιή“ΚΟφΥυ‘ΎΩΧΕ»ΓΘ
(1)ΒΈΕ®≤ΌΉςΒΡ’ΐ»ΖΥ≥–ρ «(”Ο–ρΚ≈Χν–¥)__________ΘΜΗΟΒΈΕ®≤ΌΉς÷–―Γ”ΟΒΡ÷Η ΨΦΝ «Ζ”ΧΣΘ§‘ρ‘ΎG≤ΌΉς÷–»γΚΈ»ΖΕ®ΒΈΕ®÷’ΒψΘΩ____________ΓΘ
(2)Φν ΫΒΈΕ®Ιή”Ο’τΝσΥ°»σœ¥ΚσΘ§Έ¥”Ο±ξΉΦ“Κ»σœ¥ΒΦ÷¬ΒΈΕ®ΫαΙϊ________ (ΧνΓΑΤΪ–ΓΓ±ΓΔΓΑΤΪ¥σΓ±ΜρΓΑ≤Μ±δΓ±)
(3)ΒΈΕ®«ΑΦν ΫΒΈΕ®ΙήΦβΉλ≤ΩΖ÷”–Τχ≈ίΘ§ΒΈΕ®ΚσΤχ≈ίœϊ ßΘ§‘ρΫαΙϊΜαΒΦ÷¬≤βΒΟΒΡœΓH2SO4»ή“Κ≈®Ε»≤βΕ®÷Β__________(―ΓΧνΓΑΤΪ¥σΓ±ΓΑΤΪ–ΓΓ±ΜρΓΑΈό”ΑœλΓ±Θ§œ¬Ά§)ΘΜ»τΒΈΕ®«Α―ω ”Φν ΫΒΈΕ®ΙήΩΧΕ»œΏΘ§ΒΈΕ®÷’ΝΥΗ© ”ΩΧΕ»œΏΘ§Μα ΙΒΈΕ®ΫαΙϊ__________ΘΜ
(4)ΦΤΥψ¥ΐ≤βΝρΥα(œΓ Ά«ΑΒΡΝρΥα)»ή“ΚΒΡΈο÷ ΒΡΝΩ≈®Ε»__________molΓΛLΘ≠1
(5)–¥≥ω”ΟœΓΝρΥα÷–ΚΆBa(OH)2»ή“Κ ±ΒΡάκΉ”ΖΫ≥Χ ΫΘΚ_____________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΡ≥Ά§―ß≤…”ΟΝρΧζΩσ±Κ…’»Γ»ΓΝρΚσΒΡ…’‘ϋ(÷ς“Σ≥…Ζ÷ΈΣFe2O3ΓΔSiO2ΓΔAl2O3Θ§≤ΜΩΦ¬«ΤδΥϊ‘”÷ )÷Τ»ΓΤΏΥ°ΚœΝρΥα―«Χζ(FeSO4ΓΛ7H2O)Θ§…ηΦΤΝΥ»γΆΦΝς≥ΧΘΚ
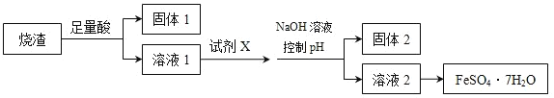
œ¬Ν–ΥΒΖ®≤Μ’ΐ»ΖΒΡ «Θ® Θ©
A.»ήΫβ…’‘ϋ―ÔϹψΝΩΝρΥαΘ§ ‘ΦΝX―Γ”ΟΧζΖέ
B.ΙΧΧε1÷–“ΜΕ®Κ§”–SiO2Θ§ΩΊ÷ΤpH «ΈΣΝΥ ΙAl3+ΉΣΜ·ΈΣAl(OH)3Θ§Ϋχ»κΙΧΧε2
C.¥”»ή“Κ2ΒΟΒΫFeSO4ΓΛ7H2O≤ζΤΖΒΡΙΐ≥Χ÷–Θ§–κΩΊ÷ΤΧθΦΰΖά÷ΙΤδ―θΜ·ΚΆΖ÷Ϋβ
D.»τ‘Ύ»ή“Κ1÷–÷±Ϋ”Φ”NaOH÷ΝΙΐΝΩΘ§ΒΟΒΫΒΡ≥ΝΒμ”ΟΝρΥα»ήΫβΘ§Τδ»ή“ΚΨ≠ΫαΨßΖ÷άκΩ…ΒΟΒΫFeSO4ΓΛ7H2O
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΥφΉ≈ άΫγΙΛ“ΒΨ≠ΦΟΒΡΖΔ’ΙΓΔ»ΥΩΎΒΡΨγ‘ωΘ§»Ϊ«ρΡή‘¥Ϋτ’≈ΦΑ άΫγΤχΚρΟφΝΌ‘Ϋά¥‘Ϋ―œ÷ΊΒΡΈ ΧβΘ§»γΚΈΫΒΒΆ¥σΤχ÷–CO2ΒΡΚ§ΝΩΦΑ”––ßΒΊΩΣΖΔάϊ”ΟCO2“ΐΤπΝΥ»Ϊ άΫγΒΡΤ’±ι÷Ί ”ΓΘ
Θ®1Θ©»γΆΦΈΣCΦΑΤδ―θΜ·ΈοΒΡ±δΜ·ΙΊœΒΆΦΘ§»τΔΌ±δΜ· «÷ΟΜΜΖ¥”ΠΘ§‘ρΤδΜ·―ßΖΫ≥Χ ΫΩ…ΈΣ___ΓΘ
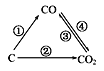
Θ®2Θ©“ΜΕ®ΧθΦΰœ¬Θ§‘ΎΟή±’»ίΤς÷–ΖΔ…ζΖ¥”ΠCO2(g)ΘΪC(s)![]() 2CO(g)¥οΒΫΤΫΚβΘ§Ρή ΙΤΫΚβœρ’ΐΖ¥”ΠΖΫœρ“ΤΕ·ΒΡ”–__(ΧνΉ÷ΡΗ)ΓΘ
2CO(g)¥οΒΫΤΫΚβΘ§Ρή ΙΤΫΚβœρ’ΐΖ¥”ΠΖΫœρ“ΤΕ·ΒΡ”–__(ΧνΉ÷ΡΗ)ΓΘ
A.±Θ≥÷ΤδΥϊΧθΦΰ≤Μ±δΘ§‘ω¥σ―Ι«Ω
B.±Θ≥÷»ίΤςΉήΧεΜΐ≤Μ±δΘ§Ά®»κ…ΌΝΩAr
C.‘ωΦ”ΧΦΒΡ”ΟΝΩ
D.±Θ≥÷ΤδΥϊΧθΦΰ≤Μ±δΘ§…ΐΗΏΈ¬Ε»
Θ®3Θ©ΗυΨίœ¬Ν–3Ηω»»Μ·―ßΖ¥”ΠΖΫ≥Χ ΫΘΚ
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΓςH=-24.8kJ/mol
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) ΓςH=-47.2kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΓςH=+640.4kJ/mol
–¥≥ωCOΤχΧεΜΙ‘≠FeOΙΧΧεΒΟΒΫFeΙΧΧεΚΆCO2ΤχΧεΒΡ»»Μ·―ßΖ¥”ΠΖΫ≥Χ ΫΘΚ__ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΦΉΓΔ““ΓΔ±ϊ»ΐ÷÷”–ΜζΜ·ΚœΈοΒΡΦϋœΏ Ϋ»γΆΦΥυ ΨΓΘœ¬Ν–ΥΒΖ®¥μΈσΒΡ «

A. ΦΉΓΔ““ΒΡΜ·―ß ΫΨυΈΣC8H14
B. ““ΒΡΕ଻¥ζΈοΙ≤”–7÷÷Θ®≤ΜΩΦ¬«ΝΔΧε“λΙΙΘ©
C. ±ϊΒΡΟϊ≥ΤΈΣ““±ΫΘ§ΤδΖ÷Ή”÷–Υυ”–ΧΦ‘≠Ή”Ω…ΡήΙ≤ΤΫΟφ
D. ΦΉΓΔ““ΓΔ±ϊΨυΡή ΙΥα–‘ΗΏΟΧΥαΦΊ»ή“ΚΆ …Ϊ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν– Β―ι’ΐ»ΖΒΡ «Θ® Θ©
A. ’τΖΔΓΔ≈®ΥθΓΔΫαΨß
B. Φλ≤ιΉΑ÷ΟΤχΟή–‘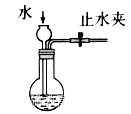
C. ΧΦΥα«βΡΤ»»Ζ÷Ϋβ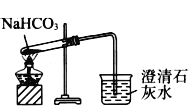
D. Ζ÷άκΖ–Βψ≤ΜΆ§«“ΜΞ»ήΒΡ“ΚΧεΜλΚœΈο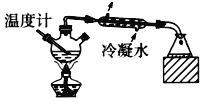
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΟß≤ίΥαΩ…”Ο”ΎΚœ≥…“©Έο¥οΖΤΘ§ΤδΫαΙΙΦρ Ϋ»γΆΦΥυ ΨΓΘœ¬Ν–ΙΊ”ΎΟß≤ίΥαΒΡΥΒΖ®’ΐ»ΖΒΡ «Θ® Θ©
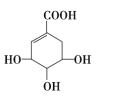
A.Ζ÷Ή”÷–Υυ”–ΧΦ‘≠Ή”Ι≤ΤΫΟφ
B.Ζ÷Ή” ΫΈΣC7H10O5Θ§ τ”ΎΖΦœψΉεΜ·ΚœΈο
C.Ζ÷Ή”÷–Κ§”–3÷÷ΙΌΡήΆ≈Θ§ΡήΖΔ…ζΦ”≥…ΓΔ―θΜ·ΓΔ»Γ¥ζΖ¥”Π
D.1molΟß≤ίΥα”κΉψΝΩΒΡNaHCO3»ή“ΚΖ¥”ΠΩ…Ζ≈≥ω4molCO2ΤχΧε
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΘ®1Θ©Ρ≥―–ΨΩ–‘―ßœΑ–ΓΉι…ηΦΤΝΥ»γΆΦΥυ ΨΉΑ÷ΟΧΫΨΩΗ÷ΧζΒΡΗ· ¥”κΖάΜΛΓΘ
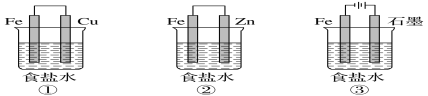
ΈΣΖά÷ΙΫπ τFe±ΜΗ· ¥Θ§Ω…“‘≤…”Ο…œ ω________Θ®ΧνΉΑ÷Ο–ρΚ≈Θ©ΉΑ÷Ο‘≠άμΫχ––ΖάΜΛΘΜΉΑ÷ΟΔέ÷–ΉήΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ_________ΓΘ
Θ®2Θ©ΈΣ¥Πάμ“χΤς±μΟφΒΡΚΎΑΏΘ®Ag2SΘ©Θ§ΫΪ“χΤςΫΰ”Ύ¬Ν÷ »ίΤςάοΒΡ ≥―ΈΥ°÷–≤Δ”κ¬ΝΫ”¥ΞΘ§Ag2SΉΣΜ·ΈΣAgΘ§ ≥―ΈΥ°ΒΡΉς”ΟΈΣ__________ΓΘ
Θ®3Θ©Ρ…ΟΉΦΕCu2O”…”ΎΨΏ”–”≈ΝΦΒΡ¥ΏΜ·–‘ΡήΕχ ήΒΫΙΊΉΔΘ§≤…”Οκ¬(N2H4)»ΦΝœΒγ≥ΊΈΣΒγ‘¥Θ§”ΟάκΉ”ΫΜΜΜΡΛΩΊ÷ΤΒγΫβ“Κ÷–c(OHΘ≠)÷Τ±ΗΡ…ΟΉCu2OΘ§ΤδΉΑ÷Ο»γΆΦΦΉΓΔ““ΓΘ
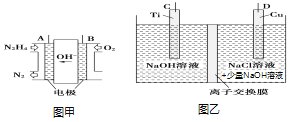
ΔΌ…œ ωΉΑ÷Ο÷–DΒγΦΪ”Πͧ۔ꬻΦΝœΒγ≥ΊΒΡ________ΦΪΘ®ΧνΓΑAΓ±ΜρΓΑBΓ±Θ©ΓΘ
ΔΎΗΟΒγΫβ≥ΊΒΡ―τΦΪΖ¥”Π ΫΈΣ_______ΓΘ
ΔέΒ±Ζ¥”Π…ζ≥…14.4 g Cu2O ±Θ§÷Ν…Ό–η“Σκ¬________molΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ«κΑ¥“Σ«σΜΊ¥πœ¬Ν–Έ ΧβΘΚ
(1)25 Γφ ±Θ§œρ¥ΩΥ°÷–Φ”»κ…ΌΝΩΧΦΥαΡΤΙΧΧεΘ§ΒΟΒΫpHΈΣ11ΒΡ»ή“ΚΘ§ΤδΥ°ΫβΒΡάκΉ”ΖΫ≥Χ ΫΈΣ_____________Θ§”…Υ°Βγάκ≥ωΒΡc(OHΘ≠)ΘΫ________molΓΛLΘ≠1ΓΘ
(2)Βγάκ≥Θ ΐ «ΚβΝΩ»θΒγΫβ÷ Βγάκ≥ΧΕ»«Ω»θΒΡΈοάμΝΩΓΘ“―÷ΣΘΚ
Μ·―ß Ϋ | Βγάκ≥Θ ΐ(25 Γφ) |
HCN | KΘΫ4.9ΓΝ10Θ≠10 |
CH3COOH | KΘΫ1.8ΓΝ10Θ≠5 |
H2CO3 | K1ΘΫ4.3ΓΝ10Θ≠7ΓΔK2ΘΫ5.6ΓΝ10Θ≠11 |
ΔΌ25 Γφ ±Θ§”–Β»pHΒΡa.NaCN»ή“ΚΓΔb.Na2CO3»ή“ΚΚΆc.CH3COONa»ή“ΚΘ§»ΐ»ή“ΚΒΡ≈®Ε»”…¥σΒΫ–ΓΒΡΥ≥–ρΈΣ___________________________ΓΘ(”Οa b c±μ Ψ)
ΔΎœρNaCN»ή“Κ÷–Ά®»κ…ΌΝΩΒΡCO2Θ§ΖΔ…ζΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΈΣ_________ΓΘ
(3) “Έ¬ ±Θ§œρ100mL 0.1mol/L NH4HSO4»ή“Κ÷–ΒΈΦ”0.1mol/L NaOH»ή“ΚΘ§ΒΟΒΫ»ή“ΚpH”κNaOH»ή“ΚΧεΜΐΒΡΙΊœΒ«ζœΏ»γΆΦΥυ ΨΘΚ
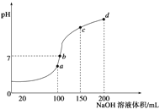
‘Ζ÷ΈωΆΦ÷–aΓΔbΓΔcΓΔdΥΡΗωΒψΘ§Υ°ΒΡΒγάκ≥ΧΕ»Ήν¥σΒΡ «________ΘΜ‘ΎbΒψΘ§»ή“Κ÷–ΗςάκΉ”≈®Ε»”…¥σΒΫ–ΓΒΡ≈≈Ν–Υ≥–ρ «_____________________________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΑΌΕ»÷¬–≈ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com