
| �� | ����ƽ�ⳣ��K |
| CH3COOH | 1.76��10- |
| H2CO3 | K1=4.31��10-7 K2=5.61��10-1 |
| H3PO4 | K1=7.52��10-3 K2=6.23��10-8 K3=2.20��10-1 |
| c(H +)?C(CH 3COO -) |
| C(CH 3COOH) |
 H++HCO3-��HCO3-
H++HCO3-��HCO3- H++CO32-��
H++CO32-�� | c(H +)?C(CH 3COO -) |
| C(CH 3COOH) |
| c����c�� |
| c-c�� |
| c�� 2 |
| 1-�� |
| c�� 2 |
| 1-�� |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������Cu��Cuԭ�Ӷѻ���ʽΪ�����������ܶѻ���ÿ��Cuԭ�ӵ���λ����Ϊ12 |
| B��������۵㣺SiC��CCl4��P4��SO2 |
| C�����ԣ�HClO4��HClO3��HClO |
| D���������ɴ�С��NaF��NaCl��NaBr��NaI |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
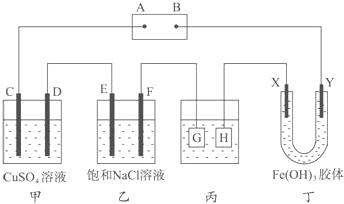
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ǰ20 min��ƽ����Ӧ����v��C��=0.1 mol/��L?min�� |
| B��A��ת����Ϊ50% |
| C��C��ƽ��Ũ��c��C��=4 mol/L |
| D��B��ƽ��Ũ��c��B��=1.5 mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����ʵ���Ũ�Ⱥ��������ͬ������ʹ�����Һ����������п��Ӧʱ����ʼʱ���߲���H2���ʻ������ |
| B��100 mL 1 mol?L-1�������50 mL 2 mol?L-1�����ᣬ�ֱ���������п��Ӧʱ�����߷ų�H2���ʺ���������� |
| C��100 mL pH=3��H2SO4��HCl��Һ��������п��Ӧ�ų�H2��������� |
| D��100 mL pH=3�������������Һ��������п��Ӧ������H2��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 +R
+R| һ������ |
| ��Ӧ�� |
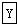 +R
+R| һ������ |
| ��Ӧ�� |
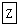
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 1 |
| 3 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com