
 和
和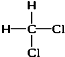
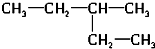 和
和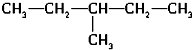 ⑦CH2=CH-CH2CH3和 CH3-CH=CH-CH3.
⑦CH2=CH-CH2CH3和 CH3-CH=CH-CH3. 分析 (1)同分异构体是指分子式相同,结构不同的有机物;
(2)同素异形体是指同种元素组成的不同单质;
(3)同位素是指质子数相同,中子数不同的同种元素的不同原子;
(4)同种物质是指分子式和结构式完全相同的物质;
解答 解:(1)同分异构体:分子式相同结构不同的化合物,⑤(CH3)2CHCH(CH3)2 和(CH3)2CH(CH2)2CH3分子式相同结构不同属于同分异构体,⑦CH2=CH-CH2CH3和 CH3-CH=CH-CH3.分子式相同结构不同属于同分异构体,
故答案为:⑤⑦;
(2)同素异形体:同种元素组成的不同单质,则④石墨和金刚石是碳元素的不同单质属于同素异形体,故答案为:④;
(3)同位素:质子数相同中子数不同的同一元素的原子互称同位素,则③35Cl和37Cl 互为同位素,故答案为:③;
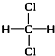
(4)甲烷中四个氢原子是等效的,所以任意两个被Cl代替的结构只有一种,即属于同一种物质的是② 和
和 ,
,
⑥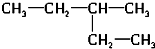 和
和 中物质均为3-甲基戊烷,是同一种物质,
中物质均为3-甲基戊烷,是同一种物质,
故答案为:②;⑥;
点评 本题考查了几种常见的化学用语,难度不大,解答时注意从其概念的内涵与外延出发,缜密思考,正确解答.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:填空题
| A | B | ||||||
| D | E | F | |||||
| C | G | H |
 ;
; +HNO3$→_{50~60℃}^{浓硫酸}$
+HNO3$→_{50~60℃}^{浓硫酸}$ +H2O,反应类型取代反应.
+H2O,反应类型取代反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-═CO32-+H2O | |
| B. | Cl2通入水中:Cl2+H2O═2H++Cl-+ClO- | |
| C. | 用氯化铁溶液腐蚀印刷线路板上的铜:Fe3++Cu═Fe2++Cu2+ | |
| D. | 明矾溶液与足量的氢氧化钡溶液混合:Al3++2SO42-+2Ba2++4OH-═AlO2-+2BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | ① | ② | ③ | 实验结论 |  |
| A | 稀硝酸 | Na2S | AgNO3与 AgCl的浊液 | Ksp(AgCl)>Ksp(Ag2S) | |
| B | 浓硫酸 | 无水 乙醇 | 溴水 | 有乙烯生成 | |
| C | 稀盐酸 | Na2SO3 | Ba(NO3)2 溶液 | SO2与可溶性钡盐均可以生成白色沉淀 | |
| D | 稀硫酸 | Na2CO3 | Na2SiO3 溶液 | 酸性: 稀硫酸>碳酸>硅酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝放入烧碱溶液中溶解:2Al+2OH-+2 H2O═2 AlO2-+3H2↑ | |
| B. | 碳酸钙溶于醋酸溶液:CaCO3+2H+═Ca2++CO2↑+H2O | |
| C. | 稀硫酸中加氢氧化钡溶液至中性:H++OH-═H2O | |
| D. | NaHCO3溶液中加入稀盐酸:CO32-+2H+═CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO作氧化剂,具有氧化性 | |
| B. | HCl是还原产物 | |
| C. | 反应中H2O提供了氧原子,因此H2O是氧化剂 | |
| D. | 生成22.4 L CO2(标准状况)时,转移的电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 锌的质量(g) | 锌的形状 | 温度(℃) | 溶解于酸所需的时间(s) | |
| A | 2 | 薄片 | 5 | 400 |
| B | 2 | 薄片 | 15 | 200 |
| C | 2 | 薄片 | 25 | 100 |
| D | 2 | 薄片 | 35 | 50 |
| E | 2 | 薄片 | 45 | 25 |
| F | 2 | 粉末 | 15 | 5 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
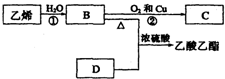 已知乙烯能发生以下转化:
已知乙烯能发生以下转化:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲酸 | B. | 乙酸 | C. | 丙酸 | D. | 乙二酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com