
【题目】已知某化学反应的平衡常数表达式为K=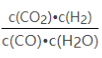 ,在不同的温度下该反应的平衡常数如下表:
,在不同的温度下该反应的平衡常数如下表:

下列有关叙述不正确的是( )
A. 该反应的化学方程式是CO(g)+H2O(g)![]() CO2(g)+H2(g)
CO2(g)+H2(g)
B. 上述反应的正反应是放热反应
C. 若在一定体积的密闭容器中通入CO2和H2各1mol,5 min后温度升高到830℃,此时测得CO2为0.4 mol时,该反应达到平衡状态
D. 若平衡浓度符合下列关系式: ![]() ,则此时的温度为1000℃
,则此时的温度为1000℃
【答案】C
【解析】A、根据化学平衡常数的定义,此化学反应方程式为CO(g)+H2O(g) ![]() CO2(g)+H2(g),故A说法正确;B、化学平衡常数只受温度的影响,根据表格中数据,随着温度的升高,化学平衡常数减小,推出此反应的正反应属于放热反应,故B说法正确;C、
CO2(g)+H2(g),故A说法正确;B、化学平衡常数只受温度的影响,根据表格中数据,随着温度的升高,化学平衡常数减小,推出此反应的正反应属于放热反应,故B说法正确;C、
CO(g)+H2O(g) ![]() CO2(g)+H2(g)
CO2(g)+H2(g)
起始: 0 0 1 1
变化: x x x x
平衡: x x 1-x 1-x ,830℃时达到平衡,根据化学平衡常数的定义,(1-x)2/x2=1,解得x=0.5mol,故C说法错误;D、根据![]() ,推出化学平衡常数K=3/5=0.6mol,根据表格数据此时温度为1000℃,故D说法正确。
,推出化学平衡常数K=3/5=0.6mol,根据表格数据此时温度为1000℃,故D说法正确。


科目:高中化学 来源: 题型:
【题目】肼(N2H4)是一种重要的化工原料,既可用于制药,又可用作火箭燃料。回答下列问题:
(1)已知反应的热化学方程式如下:
①N2H4(g)![]() N2(g)+2H2(g) △H1;
N2(g)+2H2(g) △H1;
②N2(g)+3H2(g)![]() 2NH3(g) △H2。
2NH3(g) △H2。
反应热△H1 _____(填“大于”或“小于”) △H2。向2 L的恒容密闭容器中充入1 mol N2H4,发生反应①,![]() (用x表示)与时间的关系如图1所示,则该温度下,反应①的平衡常数K=___________________。
(用x表示)与时间的关系如图1所示,则该温度下,反应①的平衡常数K=___________________。

(2)肼在另一条件下也可达到分解平衡,同时生成两种气体,且其中一种气体能使湿润的红色石蕊试纸变蓝。图2为平衡体系中肼的体积分数与温度、压强的关系。
①该反应的化学方程式为________________________________________。
②p2_______ (填“大于”或“小于”) p1。
③图中N2H4的平衡体积分数随温度升高而降低,其原因是__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可用如图所示的装置制取少量乙酸乙酯(酒精灯等在图中均已略去)。请回答下列问题:
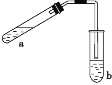
(1)试管a中需要加入浓硫酸、冰醋酸和乙醇各2 mL,加入的操作顺序是 。
(2)为防止a中的液体在实验时发生暴沸,在加热前应采取的措施是 。
(3)写出实验中加热试管的目的:① ;② 。
(4)试管b中盛有饱和Na2CO3溶液,其作用是 。
(5)反应结束后,振荡试管b,静置,观察到的现象是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若有A、B、C三种烃的衍生物,相互转化关系如下:
1,2二溴乙烷![]() 气体D
气体D![]() A
A![]() B
B![]() C
C
C跟石灰石反应产生使澄清石灰水变浑浊的气体。
(1)A、B、C中所含官能团的名称是 、 、 。
(2)书写下列反应的化学方程式
A→B的化学方程式为: ___________________
B→C的化学方程式为: ___________________
B→A的化学方程式为: ___________________
(3)上述A、B、C、D四种物质还原性最强的是 (填名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将 20.0 g 质量分数为 14.0%的 KNO3溶液与 30.0 g 质量分数为 24.0%的 KNO3溶液混合,得到的密度为1.15 g/cm3的混合溶液。计算:
(1)混合后溶液的质量分数_________。
(2)混合后溶液的物质的量浓度_______。
(3)在1000g水中需溶解______molKNO3才能使其浓度恰好与上述混合后溶液的浓度相等?
(4)标况下44.8LHCl溶于水配成500mL溶液。计算:
①HCl的物质的量____________________;
②所得溶液中溶质的物质的量浓度____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设计如图所示的装置研究电化学原理,下列叙述错误的是( )
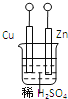
A. a、b不连接时,只锌片上有气泡逸出,锌片逐渐溶解
B. a和b用导线连接时,H+从铜片上获得锌失去的电子
C. a和b是否用导线连接,装置中所涉及的化学反应都相同
D. a和b是否用导线连接,装置中都是化学能转变为电能过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】检验SO2气体中是否混有CO2气体,可采用的方法是( )
A.通过品红溶液
B.通过澄清石灰水
C.先通过NaOH溶液,再通过澄清石灰水
D.先通过足量酸性KMnO4溶液,再通过澄清石灰水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阅读题目,回答问题。
(1)已知: P4(s)+6Cl2(g)=4PCl3(g) ΔH=akJ·mol-1, P4(s)+10Cl2(g)=4PCl5(g) ΔH=b kJ·mol-1,P4具有正四面体结构,PCl5中P—Cl键的键能为c kJ·mol-1,PCl3中P—Cl键的键能为1.2c kJ·mol-1。请回答:PCl3(g)和氯气反应生成PCl5(g)的热化学方程式为________________________________,Cl—Cl 键的键能为_________________________。
(2)离子液体是一种室温熔融盐非水体系。由有机阳离子、Al2Cl7-利AlCl4-组成的离子液体作电解液时,可在钢制品上电镀铝。则钢制品应接电源的__________极,已知电镀过程中不产生其他离子且有机阳离子不参与电极反应,阴极电极反应式为_________________________。
(3)人工肾脏可用间接电化学方法除去代谢产物中的尿素,原理如图
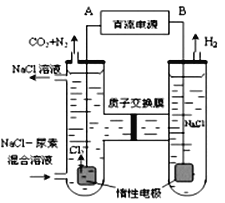
①电源的负极为_____________(填“A”或“B”)。
②阳极室中发生的反应为_____________________,______________________。
③电解结束后,阴极室溶液的pH 与电解前相比将____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、Q、R皆为前20号元素,其原子半径与主要化合价的关系如图所示。下列说法错误是

A. Q位于第三周期IA族
B. X、Y、Z三种元素组成的化合物可能是盐或碱
C. 简单离子半径:M->Q+>R2+
D. Z与M的最高价氧化物对应水化物均为强酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com