
已知:①N2(g)+3H2(g) 2NH3(g)△H<0,
2NH3(g)△H<0,
②2SO2(g)+O2(g) 2SO3(g)△H<0.请回答下列问题:
2SO3(g)△H<0.请回答下列问题:
(1)从影响化学反应速率和化学平衡的因素分析,要有利于NH3和SO3的生成,理论上应采取的措施是适当温度、高压、催化剂.实际生产中采取的措施,合成氨是 ,合成SO3是 .
(2)在合成氨的工业生产中,要分离出氨,目的是 ;而合成SO3的过程中,则不需要分离出SO3,原因是 .
(3)将0.050mol SO2(g)和0.030mol O2(g)放入容积为1L的密闭容器中,反应②在一定条件下达到平衡,测得c(SO3)=0.040mol•L﹣1.计算该条件下反应②的平衡常数K= .
考点:
用化学平衡常数进行计算;合成氨条件的选择.
分析:
(1)实际生产中合成氨采取的措施是20Mpa~50Mpa、500℃的高温、铁触媒作催化剂;
实际生产中合成SO3采取的措施是常压、400℃~500℃的高温、V2O5作催化剂;
(2)将生成的氨液化并及时从体系中分离出来,减少生成物浓度,平衡正向进行,提高原料的转化率;
合成SO3的过程中,由于二氧化硫的转化率已经很高,分离出SO3对二氧化硫的转化率基本无影响;
(3)依据化学平衡三段式求出各物质的浓度,再根据平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积进行计算.
解答:
解:(1)实际生产中合成氨采取的措施是20Mpa~50Mpa、500℃的高温、铁触媒作催化剂;
实际生产中合成SO3采取的措施是常压、400℃~500℃的高温、V2O5作催化剂;
故答案为:20Mpa~50Mpa、500℃的高温、铁触媒作催化剂;常压、400℃~500℃的高温、V2O5作催化剂;
(2)将生成的氨液化并及时从体系中分离出来,减少生成物浓度,平衡正向进行,提高原料的转化率;
合成SO3的过程中,由于二氧化硫的转化率已经很高,分离出SO3对二氧化硫的转化率基本无影响,故合成SO3的过程中,则不需要分离出SO3,
故答案为:减少生成物浓度,平衡正向进行,提高原料的转化率;二氧化硫的转化率已经很高,分离出SO3对二氧化硫的转化率基本无影响;
(3)将0.050molSO2(g)和0.030molO2(g)放入容积为1L的密闭容器中,反应:2SO2(g)+O2(g)⇌2SO3(g) 在一定条件下达到平衡,测得c(SO3)=0.040mol•L﹣1,则
2SO2(g)+O2(g)⇌2SO3(g)
起始量(mol/L) 0.05 0.03 0
变化量(mol/L) 0.04 0.02 0.04
平衡量(mol/L)0.01 0.01 0.04
平衡常数=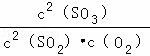 =
=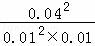 =1.6×103;
=1.6×103;
故答案为:1.6×103.
点评:
本题考查工业合成氨和合成SO3的相关知识,以及平衡常数的相关计算,难度中等.要注意基础知识的积累与比较.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
某溶液仅含Fe2+、Na+、Al3+、Ba2+、SO42﹣、NO3﹣、Cl﹣中的4种离子,所含离子的物质的量均为1mol.若向该溶液中加入过量的稀硫酸,有气体产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解).下列说法不正确的是( )
A. 该溶液中所含的离子是:Fe2+、Na+、SO42﹣、NO3﹣
B. 若向该溶液中加入过量的稀硫酸,产生的气体在空气中能变成红棕色
C. 若向该溶液中加人过量的稀硫酸和KSCN溶液,溶液显血红色
D. 若向该溶液中加入足量的NaOH溶液,充分反应后,过滤、洗涤、灼烧,最终所得固体的质量为72g
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )
|
| A. | 等质量的乙醛和乙酸乙酯完全燃烧时消耗氧气的量不相等 |
|
| B. | 淀粉水解的最终产物在加热条件下可与新制氢氧化铜反应生成砖红色沉淀 |
|
| C. | 可用饱和碳酸钠溶液除去乙酸乙酯中的乙酸 |
|
| D. | 2﹣氯﹣2﹣甲基丙烷在氢氧化钠的醇溶液中加热可生成甲基丙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
1791年,法国医生路布兰首先获得制碱专利,以食盐、浓硫酸、石灰石、煤为原料制碱,该方法分三步:
①用NaCl与H2SO4反应制Na2SO4:2NaCl+H2SO4═Na2SO4+2HCl↑
②用焦炭还原Na2SO4制Na2S:Na2SO4+4C═Na2S+4CO↑
③用硫化钠与石灰石反应制Na2CO3:Na2S+CaCO3═Na2CO3+CaS
下列说法正确的是( )
|
| A. | ②③两步都是氧化还原反应 |
|
| B. | 只有第②步是氧化还原反应 |
|
| C. | 该方法对生产设备基本没有腐蚀 |
|
| D. | 该方法对环境污染较小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.将钠放入水中,钠将沉在水底
B.将一小块钠放在稀盐酸中,钠将与水反应生成NaOH和H2,生成的NaOH再与HCl反应生成NaCl和H2O
C.将一小块钠放在CuSO4溶液中发生如下反应:2Na+CuSO4═Na2SO4+Cu
D.Na2O和Na2O2中,氧元素化合价不同
查看答案和解析>>
科目:高中化学 来源: 题型:
在体积相同的两个密闭容器中分别充满O2、O3气体,当这两个容器内温度和气体密度相等时,下列说法正确的是( )
A.两种气体的压强相等 B.O2比O3质量小
C.两种气体的分子数目相等 D.两种气体的氧原子数目相等
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.摩尔是七个基本物理量之一
B.阿伏伽德罗常数是没有单位的
C.氮气的摩尔质量是28g
D.1molH2O约含有6.02×1023个水分子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com