
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解
2- 4 |
2- 3 |
2- 3 |
- 3 |
- 3 |

| 肯定存在的离子 | 肯定没有的离子 | 沉淀D | |
| 化学式或离子符号 | HCO3- HCO3- |
Br- Br- |
BaSO4 BaSO4 |
2- 3 |
2- 4 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
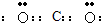
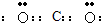


查看答案和解析>>
科目:高中化学 来源:2013-2014学年浙江省金华十校高考模拟考试理综化学试卷(解析版) 题型:填空题
某化合物M(式量为80)俗称黑肥宝,它由原子序数不大于20的X、Y、Z三种元素组成,X、Y、Z的原子序数依次增大,其关系为Z=X+2Y。X、Y是同周期相邻的两种元素。M微溶于水,在常温下与水作用发生缓慢水解,最终产物为一种白色沉淀A与气体B,该气体能使湿润的红色石蕊试纸变蓝,A在高温条件下可分解产生一种有温室效应的气体。(注:以下回答若涉及到具体物质均用相应的化学式或元素符号表示)
(1)化合物M的化学式为? ??????? ;Z的原子结构示意图为????????? 。
(2)写出下列反应的化学方程式。A在高温下分解:???????? ???????? ; M与水反应生成A和B:??????? ????????????????? 。
(3)Z的氢化物可作为一种储氢材料,写出其与水反应的化学方程式 ????????? 。
(4)储氢材料的研究很广泛。下列物质中,可作为储氢材料的是? ????????? 。(填编号)
A.Ca(OH)2? ??? B.MgH2 ??? C.O2? ??? D.LaNi5
? (5)物质B有如下转化关系: (强酸),将C和D的混气体通入NaOH溶液中恰好完全反应得到一种盐,请设计一个实验方案检验其中的阴离子?????????? 。
(强酸),将C和D的混气体通入NaOH溶液中恰好完全反应得到一种盐,请设计一个实验方案检验其中的阴离子?????????? 。
查看答案和解析>>
科目:高中化学 来源: 题型:
①A的阳离子和D的阴离子具有相同的核外电子排布,且A与B能形成组成为A2B的化合物;
②B和D属同族元素,它们能形成两种常见的化合物,且B单质与H2化合更容易;③C元素原子的最外层电子数是D元素原子的最外层电子数的![]() ,且C、D同周期,C的离子半径比B的离子半径小。
,且C、D同周期,C的离子半径比B的离子半径小。
(1)写出B元素的名称:___________。
(2)写出D元素和C元素的最高价氧化物的水化物之间反应的离子方程式:
____________________________________________。
(3)用离子方程式表示A2D水溶液呈碱性的原因:____________________________________。
(4)A离子的结构示意图__________________,A、B、C、D形成结晶盐的化学式为______________________,其用途之一是___________________________________。
(5)工业上制C单质的化学方程式:_________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com