
8.7 g MnO2和120 mL 10 mol·L-1的盐酸作用制取Cl2,把完全反应后的溶液稀释至1.0L后取出20 mL,在这20 mL的溶液中加入足量的AgNO3溶液,可得AgCl多少克?
 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源:0110 会考题 题型:实验题
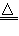 5Cl-+ClO3-+3H2O
5Cl-+ClO3-+3H2O 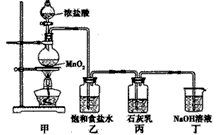
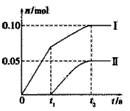
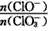 =___
=___ 查看答案和解析>>
科目:高中化学 来源:同步题 题型:计算题
查看答案和解析>>
科目:高中化学 来源:2011-2012学年江苏省扬州市邗江区蒋王中学高三(上)期中化学模拟试卷(解析版) 题型:选择题
 的数目为0.5 NA
的数目为0.5 NA查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com