
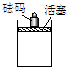
 在一定条件下,向如图容器中加入一定量的A和B,发生反应:mA+nB?pC达到平衡.
在一定条件下,向如图容器中加入一定量的A和B,发生反应:mA+nB?pC达到平衡.

科目:高中化学 来源: 题型:
| A、加入催化剂,逆反应速率不变 |
| B、增大反应体系的压强,正反应速率一定增大 |
| C、升高温度,反应速率加快,反应放出的热量减小 |
| D、若在原电池中进行,反应放出的热量不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol Na2O2含离子数为4NA |
| B、标准状况下,22.4 L 氯气与足量的氢氧化钠溶液充分反应,转移的电子数为2NA. |
| C、常温常压下,8.0g CH4中含有的氢原子数为2NA |
| D、0.1 mol/L CaCl2溶液中含氯离子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Al3+、Cl- |
| B、Al3+ |
| C、Fe2+、Cl- |
| D、Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、棕红色NO2加压后颜色先变浅后变深 |
| B、向Fe(SCN)3溶液中加入少量KSCN固体,溶液红色变浅 |
| C、把装有NO2气体的烧瓶放入冰水中,气体红棕色变深 |
| D、向新制AgCl悬浊液中滴入Na2S溶液,振荡后沉淀可以由白色变为黑色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、920 kJ |
| B、557 kJ |
| C、436 kJ |
| D、188 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、40℃时,0.005 mol?L-1 H2SO4溶液的pH为2 |
| B、往氯化铁溶液中滴加氨水来制备氢氧化铁胶体 |
| C、镀锌铁制品镀层受损后,铁制品易生锈 |
| D、已知NaCl溶液和CH3COONH4溶液均显中性,则两溶液中水的电离程度相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 弱酸 | CH3COOH | H2CO3 | HNO2 |
| 电离常数( | K=1.8×10-5 | K=4.3×10-7 K=5.6×10-11 | K=5.0×10-4 |
| c(CH3COO-) |
| c(CH3COOH) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com