
分析 蛋白质变性是指蛋白质在某些物理和化学因素作用下其特定的空间构象被改变,从而导致其理化性质的改变和生物活性的丧失,这种现象称为蛋白质变性;
能使蛋白质变性的化学方法有加强酸、强碱、尿素、乙醇、丙酮、甲醛等有机溶剂化学物质、重金属盐等;
能使蛋白质变性的物理方法有加热(高温)、紫外线及X射线照射、超声波、剧烈振荡或搅拌等.
解答 解:(1)①饱和(NH4)2SO4溶液、④饱和Na2SO4溶液、⑤饱和NaCl溶液能使蛋白质发生盐析,故答案为:①④⑤;
(2)②浓NaOH溶液、③饱和CuSO4溶液、⑥甲醛能使蛋白质发生变性,故答案为:②③⑥.
点评 本题考查蛋白质的变性,难度不大,了解蛋白质变性的常用方法,注意蛋白质变性是不可逆的.


科目:高中化学 来源: 题型:选择题
| A. | 简单辨认有味的化学药品时,将瓶口远离鼻子,用手在瓶口上方扇动,稍闻其味即可 | |
| B. | 处置实验过程产生的剧毒药品废液,稀释后用大量水冲净 | |
| C. | 金属钠着火不能用水灭火,应使用干砂灭火 | |
| D. | 危险化学品包括:爆炸品、易燃物质、自燃自热物质、氧化性气体、加压气体等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀释浓硫酸时,将浓硫酸缓慢地沿着量筒内壁倒入蒸馏水中,并用玻璃棒进行搅拌 | |
| B. | 实验室的酒精灯着火时,应该立即往上撒水 | |
| C. | 实验室制氧气,组装好装置后,应该先检查装置的气密性 | |
| D. | 过滤时,若滤液浑浊,则将滤液放入蒸发皿中进行蒸发结晶 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (1)A.NH3 B.SO3 C.Cl2 D.BaSO4 E.酒精 F.CH3COONH4
(1)A.NH3 B.SO3 C.Cl2 D.BaSO4 E.酒精 F.CH3COONH4查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
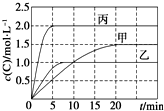 向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:A(g)+xB(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下表和如图表示:
向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:A(g)+xB(g)?2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下表和如图表示:| 容器 | 甲 | 乙 | 丙 |
| 容积 | 0.5 L | 0.5 L | 1.0 L |
| 温度/℃ | T1 | T2 | T2 |
| 反应物起始量 | 1.5 mol A 0.5 mol B | 1.5 mol A 0.5 mol B | 6.0 mol A 2.0 mol B |
| A. | 10min内甲容器中反应的平均速率v(A)=0.025 mol•L-1•min-1 | |
| B. | 由图可知:T1<T2,且该反应为吸热反应 | |
| C. | 若平衡时保持温度不变,改变容器体积平衡不移动 | |
| D. | T1℃,起始时甲容器中充入0.5 mol A、1.5 mol B,平衡时A的转化率为25% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 碳的氧化物在工业上有着广泛的应用,如CO 和H2可以合成甲醇,CO2 和NH3可以合成尿素.
碳的氧化物在工业上有着广泛的应用,如CO 和H2可以合成甲醇,CO2 和NH3可以合成尿素.| t/min | 0 | 1 | 3 | 5 |
| n(H2)/mol | 8 | 5 | 4 | 4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com