
| 选用试剂 | 实验现象 | |
| 方案1 | ||
| 方案2 |
分析 (2)①根据溴水的颜色来进行猜想;
②根据发生氧化还原反应生成Fe3+及Fe3+在水中的颜色来猜想;
(3)利用Fe3+的检验及萃取来进行实验的设计,Fe3+遇KSCN溶液变为红色,溴易溶于四氯化碳中,且四氯化碳与水不溶;
(4)①由氧化性Br2>Fe3+,则氯化亚铁溶液中加入1~2滴溴水发生氧化还原反应生成Fe3+;
②根据电子守恒进行计算.
解答 解:(2)①因溴水的颜色为黄色,则溶液呈黄色是因为含有Br2所致,故答案为:Br2;
②氧化性:Br2>Fe3+,则发生2Fe2++Br2=2Fe3++2Br-,生成Fe3+且Fe3+在水中为黄色,溶液呈黄色是因为含有Fe3+所致,故答案为:Fe3+;
(3)因Fe3+遇KSCN溶液变为红色,溴易溶于四氯化碳中,且四氯化碳与水不溶,则
| 试剂 | 实验现象 | |
| 方案1 | d | 溶液变成血红色 |
| 方案2 | b | 下层的四氯化碳溶液依然无色 |
| 试剂 | 实验现象 | |
| 方案1 | d | 溶液变成血红色 |
| 方案2 | b | 下层的四氯化碳溶液依然无色 |
点评 本题考查氧化还原反应及氧化性、还原性的比较、实验设计,学生应注意物质的性质及氧化还原反应中电子守恒来分析,题目难度中等.


 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:选择题
| A. | X-衍射实验可以区分晶体和非晶体 | B. | SiO2属于原子晶体 | ||
| C. | 金属钋是简单立方堆积 | D. | 晶格能的大小只与离子半径有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
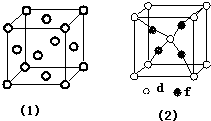 周期表前四周期的元素a、b、c、d、e、f,原子序数依次增大.a是宇宙中最丰富的元素,b的某种核素在考古时用来测定一些文物的年代,d与e同族,用e氧化物漂白的草帽日久又变成黄色;f的最外层只有1个电子,但次外层有18个电子.回答下列问题;
周期表前四周期的元素a、b、c、d、e、f,原子序数依次增大.a是宇宙中最丰富的元素,b的某种核素在考古时用来测定一些文物的年代,d与e同族,用e氧化物漂白的草帽日久又变成黄色;f的最外层只有1个电子,但次外层有18个电子.回答下列问题;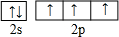 ,f在周期表中的位置是第四周期第IB族
,f在周期表中的位置是第四周期第IB族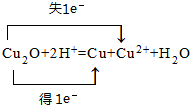 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 己烷、己烯和CCl4可以用溴水鉴别 | |
| B. | 除去甲苯中的苯乙烯(C6H5CH═CH2)可以用溴水 | |
| C. | 乙烯、聚氯乙烯和苯分子中均含有碳碳双键 | |
| D. | 乙烯和二氧化硫使溴水褪色的原理相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3v(H2)正=2v(NH3)逆 | |
| B. | a molN-N键断裂的同时,有6a mol N-H键断裂 | |
| C. | 混合气体的密度不再随时间变化 | |
| D. | 单位时间生成m mol N2的同时消耗3m mol H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ag+、K+、NO${\;}_{3}^{-}$、Cl- | B. | Mg2+、Na+、Cl-、SO${\;}_{4}^{2-}$ | ||
| C. | Ca2+、Mg2+、OH-、Cl- | D. | H+、Na+、CO${\;}_{3}^{2-}$、NO${\;}_{3}^{-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.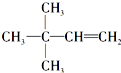 或
或 或
或 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com