
【题目】我们如何找到回家的路?荣获2014年诺贝尔生理学或医学奖的三位科学家发现大脑里的神经细胞——“位置细胞”和“网格细胞”起到了重要作用。下列叙述中正确的是
A. “位置细胞”鲜重中质量百分比最高的元素是C
B. “网格细胞”干重中质量百分比最高的元素是O
C. 上述两种细胞鲜重中原子数量最多的元素均是H
D. P和S分别是“位置细胞”中的大量元素和微量元素
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列实验操作正确的是
A. 蒸发时,将蒸发皿放置在铁架台的铁圈上直接用酒精灯外焰加热
B. 蒸馏时,温度计水银球浸入蒸馏烧瓶内液面下,冷凝水从冷凝管下口进
C. 萃取时,分别用两个烧杯从下口接收有机层和水层
D. 配制100ml 0.100 mol/L的硫酸铜溶液时,可将2.50克胆矾溶于100mL蒸馏水中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(17分)
羟甲香豆素是一种治疗胆结石的药物,合成路线如下图所示:
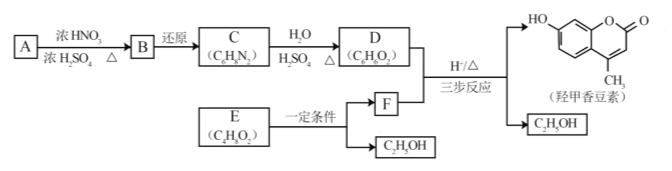
已知: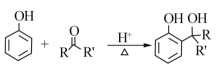
RCOOR'+R'OH![]() RCOOR'+ R'OH(R、R'、R'代表烃基)
RCOOR'+ R'OH(R、R'、R'代表烃基)
(1)A属于芳香烃,其结构简式是______________________。B中所含的官能团是________________。
(2)C→D的反应类型是___________________。
(3)E属于脂类。仅以乙醇为有机原料,选用必要的无机试剂合成E,写出有关化学方程式:______________________________。
(4)已知:2E![]() F+C2H5OH。F所含官能团有
F+C2H5OH。F所含官能团有![]() 和___________。
和___________。
(5)以D和F为原料合成羟甲香豆素分为三步反应,写出有关化合物的结构简式:

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种化工原料,在工业生产中有重要的应用。
Ⅰ.在l.0L恒容密闭容器中投入1 molCO2和2.75molH2发生反应:
CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),实验测得不同温度及压强下,平衡时甲醇的物质的量变化如图所示,下列说法正确的是_______。
CH3OH(g)+H2O(g),实验测得不同温度及压强下,平衡时甲醇的物质的量变化如图所示,下列说法正确的是_______。

A.该反应的正反应为放热反应
B.压强大小关系为pl<p2<p3
c. M点对应的平衡常数K的值约为1.04×10-2
D.在p2及512K时,图中N点v(正)<v(逆)
Ⅱ.甲醇是基本有机化工原料。甲醇及其可制得的产品的沸点如下。
名称 | 甲醇 | 二甲胺 | 二甲基甲酰胺 | 甲醚 | 碳酸二甲酯 |
结构简式 | CH3OH | (CH3)2NH | (CH3)2NCHO | CH3OCH3 | (CH3O)2CO |
沸点/℃ | 64.7 | 7.4 | 153 | -24.9 | 90 |
(1)在425℃、Al2O3做催化剂,甲醇与氨气反应可以制得二甲胺。二甲胺显弱碱性,与盐酸反应生成(CH3)2NH2Cl,溶液中各离子浓度由大到小的顺序为____________。
(2)甲醇制甲醚的化学方程式为2CH3OH![]() CH3OCH3+H2O,一定温度下,在体积为1.0L的恒容密闭容器中发生该反应。己知387℃时该反应的化学平衡常数K=4,若起始时向容器I中充入0.10molCH3OH、0.15molCH3OCH3和0.10molH2O,则反应将向______(填“正”或“逆”)反应方向进行。
CH3OCH3+H2O,一定温度下,在体积为1.0L的恒容密闭容器中发生该反应。己知387℃时该反应的化学平衡常数K=4,若起始时向容器I中充入0.10molCH3OH、0.15molCH3OCH3和0.10molH2O,则反应将向______(填“正”或“逆”)反应方向进行。
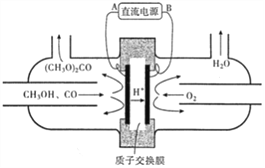
(3)以甲醇为主要原料,电化学合成碳酸二甲酯的工作原理如下图所示。
电源的负极为__________(填“A”或“B”),写出阳极的电极反应_________;若参加反应的O2为1.12m3(标准状况),则制得的碳酸二甲酯的质量为______kg。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述中正确的是( )
A. 标准状况下,22.4LCCl4含有的分子数约为6.02×1023个
B. 1L氢气一定比1L氧气质量少
C. 含有6.02×1023个Fe3+的Fe2(SO4)3中SO42﹣的物质的量为3mol
D. 1molAl3+带有的正电荷数为1.806×1024个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】非金属元素H、C、O、S、Cl能形成的化合物种类很多,单质及化合物的用途很广泛。
(1)O2的电子式为 。
(2)O、Cl两元素形成的单质和化合物常用来杀菌消毒,试举例________(化学式,任写两种)。
(3)CH3OH在常温下为液态,沸点高于乙烷的主要原因是 。
(4)Cl2是一种大气污染物,液氯储存区贴有的说明卡如下(部分):
危险性 |
|
储运要求 | 远离金属粉末、氨、烃类、醇类物质;设置氯气检测仪 |
泄漏处理 | NaOH、NaHSO3溶液吸收 |
包装 | 钢瓶 |
①用离子方程式表示“泄漏处理”中NaHSO3溶液的作用: 。
②若液氯泄漏后遇到苯,在钢瓶表面氯与苯的反应明显加快,原因是 。
③将Cl2通入适量KOH溶液中,产物中可能有KCl、KClO、KClO3。当溶液中c(Cl)∶c(ClO)=11∶1时,则c(ClO)∶c(![]() )比值等于 。
)比值等于 。
(5)镁是一种较活泼的金属, Mg与Ca类似,也能与C形成某种易水解的离子化合物。已知该化合物0.1 mol与水完全反应后,产生0.1 mol的某种气体。该气体被溴水全部吸收后,溴水增重2.6 g。请写出该水解反应方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】要检验某溶液中是否含有Cl-,可选用的试剂是 ( )
A. AgNO3溶液和稀硝酸 B. AgNO3溶液
C. AgNO3溶液和稀硫酸 D. AgNO3溶液和稀盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)相同条件下,某容器共收集到1体积CO2、3体积H2,该容器中CO2、H2的物质的量之比是__________;若该容器收集的CO2、H2两种气体所含分子数相等,则CO2、H2的质量之比是_____________。
(2)0.01 mol某物质的质量为1.08g,此物质的摩尔质量为_________。
(3)已知A是二价金属,82 g该金属的硝酸盐中含有6.02 x1023个硝酸根离子,则该硝酸盐的摩尔质量为________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com