
【题目】NH3是一种重要的工业原料。下列关于合成氨的说法中,不正确的是( )
A.工艺涉及催化技术
B.工艺涉及高温高压技术
C.原料之一的氮气来自空气
D.从合成塔出来的气体中,氨的体积分数为100%
【答案】D
【解析】
NH3是一种重要的工业原料,合成氨反应为:N2+3H2![]() 2NH3△H<0。
2NH3△H<0。
A.氮肥厂利用氮气和氢气在有铁存在的情况下合成氨,铁是该反应的催化剂,催化剂可降低反应物的活化能,提高活化分子百分数,活化分子数目增多,提高了反应速率,故A正确;
B.合成氨的过程中,为保障反应速率和限度较大、催化剂的活性大,要选择适宜的温度400~500℃,压强在20~50Mpa之间,故B正确;
C.根据工业生产中,要求经济利益最大化,空气中有大量氮气,氮气来自空气廉价,氢气来自水和碳氢化合物,故C正确;
D.该反应为可逆反应,可逆反应在一定条件下达到化学反应限度时,可逆反应到达平衡状态,正逆反应速率相等,反应物不可能完全转化,故D错误;
故选D。


科目:高中化学 来源: 题型:
【题目】工业上用铁矿石、焦炭、空气、石灰石为原料来冶炼铁。
(1)请写出用磁铁矿在高温下冶炼铁的化学方程式___________。请你用化学方法设计实验方案检验上述反应得到的固体产物中含有铁粉___________。
(2)小明同学将用冶炼所得的铁粉按下图装置来制备 Fe(OH)2,实验开始时应先_______活塞a,___________活塞 b(填“打开”或“关闭”)
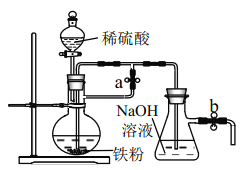
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在实验室进行铁盐与亚铁盐相互转化的实验:
实验Ⅰ:将![]() 转化为
转化为![]() 如图
如图![]()
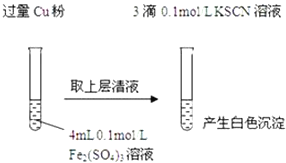
(1)Fe3+与Cu粉发生反应的离子方程式为______.
(2)探究白色沉淀产生的原因,请填写实验方案:查阅资料:
![]() 的化学性质与
的化学性质与![]() 相似,
相似,![]() 白色
白色![]()
实验方案 | 现象 | 结论 |
步骤1:取4mL ______ | 产生白色沉淀 |
|
步骤2:取 ______ | 无明显现象 |
![]() 与
与![]() 反应的离子方程式为______.
反应的离子方程式为______.
实验Ⅱ:将![]() 转化为
转化为![]()
实验方案 | 现象 |
向3mL | 溶液变为棕色,放置一段时间后,棕色消失,溶液变为黄色 |
探究上述现象出现的原因:查阅资料:![]() 棕色
棕色![]()
(3)用离子方程式解释NO产生的原因______.
(4)从化学反应速率与限度的角度对体系中存在的反应进行
反应Ⅰ:![]() 与
与![]() 反应;反应Ⅱ:
反应;反应Ⅱ:![]() 与NO反应
与NO反应
①依据实验现象,甲认为反应Ⅰ的速率比反应Ⅱ______![]() 填“快”或“慢”
填“快”或“慢”![]() .
.
②乙认为反应Ⅰ是一个不可逆反应,并通过实验证明其猜测正确,乙设计的实验方案是______.
③请用化学平衡移动原理解释溶液由棕色变为黄色的原因______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值。下列说法正确的是 ( )
A.标准状况下,0.1 mol Cl2溶于水,转移的电子数目为0.2 NA
B.常温常压下,18 g H2O中含的质子数为10 NA
C.标准状况下,11.2 L CH2Cl2中含有的分子数目为0.5 NA
D.常温常压下,2.24 L CO和CO2混合气体中含有的碳原子数目为0.1 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为几种晶体或晶胞的示意图:


请回答下列问题:
(1)上述晶体中,粒子之间以共价键结合形成的晶体是____。
(2)冰、金刚石、MgO、CaCl2、干冰5种晶体的熔点由高到低的顺序为:___。
(3)NaCl晶胞与MgO晶胞相同,NaCl晶体的晶格能___(填“大于”或“小于”)MgO晶体,原因是____。
(4)每个Cu晶胞中实际占有___个Cu原子,CaCl2晶体中Ca2+的配位数为__。
(5)冰的熔点远高于干冰,除H2O是极性分子、CO2是非极性分子外,还有一个重要的原因是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于密闭容器中的反应:2SO2(g)+O2(g)![]() 2SO3(g) △H<0,450℃时,n(SO3)和n(O2)随时间的变化关系如图所示,下列说法正确的是
2SO3(g) △H<0,450℃时,n(SO3)和n(O2)随时间的变化关系如图所示,下列说法正确的是

A.点c处反应达到平衡
B.点a的正反应速率比点b的大
C.点d (t1时刻)和点e (t2时刻)处n(SO2)不一样
D.其他条件不变,600℃时反应至t1时刻,n(SO 3)比上图中的e点值要大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列涉及有机物的性质或应用的说法不正确的是![]()
A.淀粉、纤维素、蛋白质都是天然高分子化合物
B.用于奥运“祥云”火炬的丙烷是一种清洁燃料
C.乙酸和油脂都能与氢氧化钠溶液反应
D.纤维素、蔗糖、葡萄糖和脂肪在一定条件下都可发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器内,进行反应:CO(g)+H2O(g)![]() CO2(g)+H2(g)。
CO2(g)+H2(g)。
得到如下两组数据:
实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需要的时间/min | ||
H2O | CO | H2 | CO | |||
1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
①实验1中以v(CO2)表示的反应速率为___。
②该反应的逆反应为___(填“吸”或“放”)热反应。
(2)在一容积为2L的密闭容器内加入2mol的CO和6mol的H2,在一定条件下发生如下反应:CO(g)+2H2(g)![]() CH3OH(g) △H<0该反应的逆反应速率与时间的关系如图所示:
CH3OH(g) △H<0该反应的逆反应速率与时间的关系如图所示:

①由图可知反应在t1、t3、t7时都达到平衡,而在t2、t8时都改变了条件,试从以下措施中选出适宜的改变条件:t2___、t8___。(此处两空均填下列选项字母序号)
a.增加CO的物质的量 b.加催化剂 c.升高温度 d.压缩容器体积 e.将CH3OH气体液化 f.充入氦气
②若t4时降压,t5时达到平衡,t6时增大反应物的浓度,请在图中画出t4~t6时逆应速率与时间的关系曲线___。
(3)已知反应2NO(g)+2CO(g)![]() N2(g)+2CO2(g)在100kPa下△H=-113.0kJ/mol,△S=-145.3J·mol-1·K-1。理论上,该反应在温度___(填“高于”或“低于”)___时均可自发进行。
N2(g)+2CO2(g)在100kPa下△H=-113.0kJ/mol,△S=-145.3J·mol-1·K-1。理论上,该反应在温度___(填“高于”或“低于”)___时均可自发进行。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列说法正确的是
A.c(NH4+)相同的①(NH4)2SO4、②(NH4)2CO3、③(NH4)2Fe(SO4)2、④NH4I溶液,其溶质物质的量浓度大小为④>②>③>①
B.0.2 mol·L-1 HCl溶液与等体积0.05 mol·L-1 Ba(OH)2溶液混合后,溶液的pH为1
C.NaHCO3溶液中: c(HCO3-)+ c(CO32-)+ 2c(H2CO3)=c(OH-)
D.浓度均为0.1 mol·L-1的CH3COOH、CH3COONa混合溶液中:c(CH3COO-)+c(OH-)>c(CH3COOH)+c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com