
I������̼ѭ������������ĸ߶����ӣ�����ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2��������ȫ������ձ����ӡ���������̼����������Ϊ��ѧ���о�����Ҫ���⣺
(1)����ͬ����CO��g����H2O��g���ֱ�ͨ�뵽���Ϊ2L�ĺ����ܱ�������,���з�Ӧ��
CO��g����H2O��g�� CO2��g����H2��g�����õ����¶���������
CO2��g����H2��g�����õ����¶���������
ʵ���� | �¶��� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
CO | H2O | H2 | CO | |||
1 | 650 | 4 | 2 | 1��6 | 2��4 | 6 |
2 | 900 | 2 | 1 | 0��4 | 1��6 | 3 |
��ʵ��1����v ��CO2����ʾ�ķ�Ӧ����Ϊ??????????????? ��������λС������ͬ����
���÷�ӦΪ ???? ���������������������ȷ�Ӧ��ʵ��2������ƽ�ⳣ��K=????????? ��
(2)��֪�ڳ��³�ѹ����
�� 2CH3OH(l���� 3O2(g���� 2CO2(g���� 4H2O(g��? ��H �� ��1275.6 kJ��mol
�� 2CO (g)+ O2(g���� 2CO2(g��?????????????????? ��H �� ��566.0 kJ��mol
�� H2O(g���� H2O(l��?????????????????????????? ��H �� ��44.0 kJ��mol
д���״�����ȫȼ������һ����̼��Һ̬ˮ���Ȼ�ѧ����ʽ��????????????????????? ��
II��(1)��ˮ���Ԫ�ش����dz��ḻ���Ӻ�ˮ����ȡ﮵��о�����DZ����������컯ѧ��Դ����Ҫԭ�ϡ���LiFePO4���ij�缫�Ĺ���ԭ������ͼ��ʾ��

�õ�صĵ����Ϊ�ܴ���Li+�Ĺ�����ϡ��ŵ�ʱ�õ缫�ǵ�ص�???? �������������������������õ缫��ӦʽΪ????????? ��
(2)�ô˵�ص�⺬��0.1 mol/L CuSO4��0.1 mol/L NaCl�Ļ����Һ100 mL�������·��ת����0.02 mole�����ҵ��صĵ缫��Ϊ���Ե缫�����������������ڱ�״���µ������??????? L�����������Һ��ˮϡ����1L����ʱ��Һ��pH��??????????? ��
������1����0.13mol/(L��min��(2�֣�?? ����(1�֣�?? 0.17(2�֣�
��2��CH3OH(l)+O2(g)��CO(g)+2H2O(l��? ��H ����442.8 kJ��mol (2��)
������1����(1�֣�?????? FePO4+e-+Li+��LiFePO4 (2�֣�?? ��2��0.168(2�֣�?? 2(2��)
��������
���������������1�����ɱ��������ͷ�Ӧ�Ļ�ѧ����ʽ��֪��֪�����������ʵ�����CO2�����ʵ�������ȵģ���������̼��Ũ�ȱ仯Ϊ1.6mol��2L��0.8mol/L����v=0.8mol/L��6min��0.13mol/(L��min)��
���¶����ߣ������ĺ������٣��������¶�ƽ�������ƶ�������ӦΪ���ȷ�Ӧ��
?????????????? H2O��g��+CO��g�� CO2��g��+H2��g��
CO2��g��+H2��g��
��ʼŨ�� 0.5mol/L 1mol/L ?? 0 ?? 0
ת��Ũ�� 0.2mol/L 0.2mol/l ??? 0.2mol/l 0.2mol/l
ƽ��Ũ�� 0.3mol/L 0.8mol/L ??? 0.2mol/l 0.2mol/l
��K=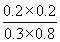 =0.17
=0.17
(2)��֪�ڳ��³�ѹ�£��� 2CH3OH(l)��3O2(g)��2CO2(g)�� 4H2O(g�� ��H ����1275.6 kJ��mol��
�� 2CO (g)+ O2(g)��2CO2(g�� ��H ����566.0 kJ��mol���� H2O(g)��H2O(l�� ��H����44.0 kJ��mol������ݸ�˹���ɿ�֪���٣���+�ۡ�4����2���õ��״�����ȫȼ������һ����̼��Һ̬ˮ���Ȼ�ѧ����ʽCH3OH(l)+O2(g)��CO(g)+2H2O(l��? ��H ����442.8 kJ��mol��
������1���ŵ�ʱ��Ԫ�صĻ��ϼ���+3�۽��͵�+2�ۣ��õ����ӣ�������������缫��ӦʽΪFePO4+e-+Li+��LiFePO4��
��2������ͭ���Ȼ��Ƶ����ʵ�������0.01mol������ͨ��0.02mol���ӣ����ͭ�����ຣ���������Ӳ��㣬����������ȫ�ŵ����Һ�е������������ַŵ硣���Ե����̿��Կ�����3���Σ��ȡµ�һ���൱���ǵ���Ȼ�ͭ���ڶ����ǵ������ͭ��������������������0.01mol��2��0.005mol�������ǣ�0.02mol��0.01mol����4��0.0025mol������������ǣ�0.005mol+0.0025mol����22.4L/mol��0.168L��������0.0025mol������ݷ�Ӧʽ2CuSO4��2H2O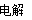 2Cu��2H2SO4��O2����֪���������ӵ����ʵ�����0.0025mol��4��0.01mol��������Ũ����0.01mol��1L��0.01mol/L����pH��2��
2Cu��2H2SO4��O2����֪���������ӵ����ʵ�����0.0025mol��4��0.01mol��������Ũ����0.01mol��1L��0.01mol/L����pH��2��
���㣺������淴Ӧ���йؼ��㡢��˹����Ӧ���Լ����ԭ�����й��ж�


 �п�������㾫��ϵ�д�
�п�������㾫��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʵ�� | �¶ȡ�C | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ���Ĵ�ʡ�����и�����һ������Կ��Ի�ѧ�Ծ��������棩 ���ͣ�������
����̼ѭ����������������ĸ߶ȹ�ע������ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2������������ȫ������ձ����ӡ�
��1���õ绡���ϳɵĴ�������̼�ܳ����д�����̼�����������ʣ������ֿ������������������ᴿ������ƽ�÷�Ӧ�Ļ�ѧ����ʽ��������ѧ��������˳�����ڴ�����ϣ�
___C��____KMnO4��____H2SO4��___CO2����____MnSO4��____K2SO4��___H2O
��2������ͬ���CO��g����H2O��g���ֱ�ͨ�˵��ݻ�Ϊ2L�ĺ����ܱ������У��������·�Ӧ��
CO��g��+H2O��g�� CO2��g��+H2��g�� �õ�������������
CO2��g��+H2��g�� �õ�������������
|
ʵ�� |
�¶ȡ� |
��ʼ��/mol |
ƽ����/mol |
�ﵽƽ������ʱ��/min |
||
|
CO |
H2O |
H2 |
CO |
|||
|
1 |
650 |
4 |
2 |
1.6 |
2.4 |
6 |
|
2 |
900 |
2 |
1 |
0.4 |
1.6 |
3 |
|
3 |
900 |
a |
b |
c |
d |
t |
��ʵ��1����v ��CO2����ʾ�ķ�Ӧ����Ϊ____��ȡ��λС������ͬ����
��ʵ��3�����£���Ӧ������������ʼ����ƽ��������֪����������������µĻ�ѧƽ�ⳣ����������ʵ��____�����ݽ��У���K=____��
��3����֪�ڳ��³�ѹ�£�
��2CH3OH��I��+3O2��g����2CO2��g��+4H2O��g�� ��H����1275.6kJ/mol
��2CO��g��+O2��g����2CO��g�� ��H����566.0kJ/mol
��H2O��g����H2O��I�� ��H����44.0kJ/mol
д���״���CH2OH������ȫȼ������һ����̼��Һ̬ˮ���Ȼ�ѧ����ʽ_ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʵ�� | �¶ȡ�C | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com