
在一真空容器中,充入10 mol N2,30 mol H2,发生反应N2(g)+3H2(g)![]() 2NH3(g),在一定条件下达到平衡时,N2的转化率为25%。若在同一容器中,在相同温度下,向容器中充入NH3,欲使达到平衡时各成分的质量分数与上述平衡相同,则起始时NH3的量和达到平衡时NH3的转化率为( )
2NH3(g),在一定条件下达到平衡时,N2的转化率为25%。若在同一容器中,在相同温度下,向容器中充入NH3,欲使达到平衡时各成分的质量分数与上述平衡相同,则起始时NH3的量和达到平衡时NH3的转化率为( )
A.20 mol、25% B.20 mol、75% C.40 mol、30% D.10mol、50%
科目:高中化学 来源: 题型:
 在100℃时,将0.40mol的二氧化氮气体充入2L真空的密闭容器中,每隔一段时间就对该容器内的物质进行分析,得到数据如表所示:
在100℃时,将0.40mol的二氧化氮气体充入2L真空的密闭容器中,每隔一段时间就对该容器内的物质进行分析,得到数据如表所示:| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
查看答案和解析>>
科目:高中化学 来源:2004全国各省市高考模拟试题汇编·化学 题型:021
一真空容器中,充入10mol N2、30mol H2,反应N2(气)+3H2(气) 2NH3(气)在一定条件下达到平衡时,N2的转化率为25%.若在同一容器中,在相同温度下,向容器中充入NH3,欲使达到平衡时各成分的质量分数与上述平衡时相同,则起始时NH3的物质的量和达到平衡时NH3的转化率为
2NH3(气)在一定条件下达到平衡时,N2的转化率为25%.若在同一容器中,在相同温度下,向容器中充入NH3,欲使达到平衡时各成分的质量分数与上述平衡时相同,则起始时NH3的物质的量和达到平衡时NH3的转化率为
[ ]
查看答案和解析>>
科目:高中化学 来源:2012-2013学年重庆市重庆一中高二上学期期中考试理科化学试卷(带解析) 题型:单选题
在一真空密闭容器中,充入10 mol N2和30 mol H2,发生N2+3H2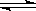 2NH3反应,在一定温度下达到平衡时,H2的转化率为25%。若在同一容器中在相同温度下充入NH3,欲达到平衡时各成分的百分含量与上述平衡相同,则起始时充入NH3的物质的量和达到平衡时NH3的转化率
2NH3反应,在一定温度下达到平衡时,H2的转化率为25%。若在同一容器中在相同温度下充入NH3,欲达到平衡时各成分的百分含量与上述平衡相同,则起始时充入NH3的物质的量和达到平衡时NH3的转化率
| A.15 mol、25% | B.20 mol、50% | C.20 mol、75% | D.40 mol、80% |
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应2A(g)![]() B(g)+3C(g),开始在一真空容器中通入一定量的A(g)达到平衡后,下列说法正确的是
B(g)+3C(g),开始在一真空容器中通入一定量的A(g)达到平衡后,下列说法正确的是
A. 测得容器内压强增大p%,A的转化率也是p%
B. 恒容容器内平衡后再充入A(g),此平衡逆向移动
C. 恒容容器内平衡后再充入等量的A(g),达到新平衡后,容器内压强p’为原平衡容器压强p的2倍
D. 恒压容器内平衡后再充入Ar(g),A的转化率不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com