
【题目】一定温度下,探究铜与稀HNO3的反应过程如图,下列说法不正确的是( )

A.过程Ⅰ中生成无色气体的离子方程式是3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O
B.步骤Ⅲ反应速率比Ⅰ快的原因是NO2溶于水,使c(HNO3)增大
C.由实验可知,NO2可能对该反应具有催化作用
D.当活塞不再移动时,再抽入空气,铜可以继续溶解
科目:高中化学 来源: 题型:
【题目】已知 4NH3+5O2 = 4NO+6H2O(g),若反应速率分别用 v(NH3)、v(O2)、v(NO)、v(H2O)表示,则正确的关系是( )
A.v(O2)=![]() v(NH3)B.v(H2O)=
v(NH3)B.v(H2O)= ![]() v(O2)C.v(H2O)=
v(O2)C.v(H2O)=![]() v(NH3)D.v(NO)=
v(NH3)D.v(NO)= ![]() v(O2)
v(O2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
Ⅰ.利用反应:6NO2+8NH3![]() 7N2+12H2O处理
7N2+12H2O处理
Ⅱ.一定条件下NO2与SO2可发生反应:NO2(g)+SO2(g)![]() SO3(g)+NO(g)-Q (Q>0)
SO3(g)+NO(g)-Q (Q>0)
Ⅲ.CO可用于合成甲醇,反应方程式为:CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)
(1)硫离子最外层电子的电子排布式为_____,氨气分子的电子式为______,氨气分子属于______分子(填“极性”或者“非极性”)。
(2)C、O、S这三种元素中属于同周期元素的非金属性由强到弱的顺序为______,能证明其递变规律的事实是_______。
a.最高价氧化物对应水化物的酸性 b.气态氢化物的沸点
c.单质与氢气反应的难易程度 d.其两两组合形成的化合物中元素的化合价
(3)对于Ⅰ中的反应,120℃时,该反应在一容积为2L的容器内反应,20min时达到平衡,10min时电子转移了1.2mol,则0~10min时,平均速率v(NO2)=_______。
(4)对于Ⅱ中的反应,将NO2与SO2以体积比1:2置于密闭容器中反应,下列能说明反应达到平衡状态的是______。
a.体系压强保持不变 b.NO2浓度保持不变
c.NO2和SO3的体积比保持不变 d.混合气体的平均相对分子质量保持不变
(5)请写出Ⅱ中反应的平衡常数表达式K=_______,如果Ⅱ中反应的平衡常数K值变大,该反应______。
a.一定向正反应方向移动 b.平衡移动时,正反应速率先减小后增大
c.一定向逆反应方向移动 d.平衡移动时,逆反应速率先增大后减小
(6)对于Ⅲ中的反应,CO在不同温度下的平衡转化率与压强的关系如图所示。实际生产条件控制在250℃、1.3×104kPa左右,简述选择此压强的理由:______。
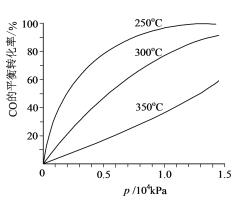
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分:
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
二 | C | N | ① | |||||
三 | ② | ③ | ④ | P | ⑤ | ⑥ |
请填写下列空白:
(1)表中元素,原子半径最大的是_______(填元素符号);①的核外电子排布式______;⑤的最外层核外电子的轨道表示式______ ;③和⑥两元素形成化合物的电子式为________。
(2)②③④三种元素最高价氧化物对应的水化物中,碱性最强的是________(填该物质化学式)。
(3)比较④、⑤两种元素的简单离子半径:___>___(填离子符号);元素④最高价氧化物对应的水化物与硝酸反应的离子方程式为____________________________。
(4)列举两个事实来证明元素①比元素⑤的非金属性强______;___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究化学能与热能的转化,某实验小组设计了如下三套实验装置:

(1)上述3个装置中,不能证明“铜与浓硝酸反应是吸热反应还是放热反应”的是___________________。
(2)某同学选用装置Ⅰ进行实验(实验前U形管里液面左右相平),在甲试管里加入适量氢氧化钡溶液与稀硫酸,U形管中可观察到的现象是___________________,说明该反应属于___________________(填“吸热”或“放热”)反应。
(3)为探究固体M溶于水的热效应,选择装置Ⅱ进行实验(反应在甲中进行)。
①若M为钠,则实验过程中烧杯中可观察到的现象是___________________;
②若观察到烧杯里产生气泡,则说明M溶于水___________________ (填“一定是放热反应”“一定是吸热反应”或“可能是放热反应”),理由是___________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置进行下列实验,能得到相应实验结论的是( )
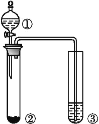
选项 | ① | ② | ③ | 实验结论 |
A | 浓硫酸 | Na2SO3 | 酸性KMnO4溶液褪色 | SO2有漂白性 |
B | 浓硫酸 | Cu | 品红溶液 | SO2具有漂白性 |
C | 稀盐酸 | 碳酸钠 | 氯化钙溶液 | CO2与CaCl2不反应 |
D | 浓硫酸 | 蔗糖 | 溴水褪色 | 浓硫酸具有脱水性、吸水性 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】芳香族化合物(C12H16O2)的性质有如下变化:
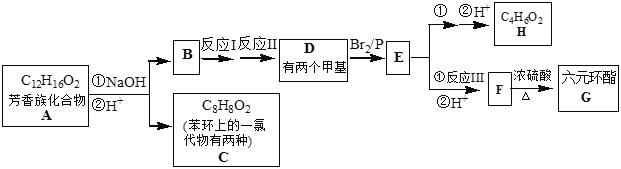
已知: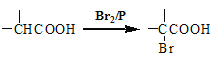
完成下列填空:
(1)E分子中所包含官能团的名称是____。
(2)D的结构简式:____。
(3)写出反应I所需的试剂和条件___;反应Ⅱ和反应Ⅲ的反应类型依次为:____、___;
(4)F生成G的化学方程式:____;
(5)已知M是C的同分异构体。M符合以下条件:
①苯环上有两个取代基(除苯环外无其他的环);②能发生水解反应③苯环上只有两种氢原子。
写出符合条件的M其中任意一种化合物的结构简式:____。
(6)运用中学化学知识及以上信息,写出由E合成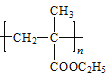 的的合成路线。__
的的合成路线。__
(合成路线常用的表示方式为:A![]() B
B![]() ……目标产物)
……目标产物)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国科学院深圳先进技术研究院研发出一种新型铝—石墨烯双离子电池(AGDIB电池),该电池以溶有六氟磷酸锂(LiPF6)的碳酸酯类溶剂为电解液,放电时合金AlLi发生去合金化反应,阴离子(PF-)从石墨烯Cx中脱嵌,进入电解质溶液。放电时其工作原理如图所示,下列说法错误的是( )
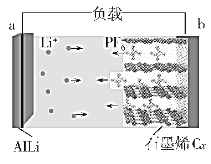
A.该电池不能用水作为电解质溶液
B.放电时,a电极的电极反应式为AlLi-e-=Li++Al
C.充电时,b电极的电极反应式为PF6--e-+Cx=CxPF6
D.废旧AGDIB电池进行“放电处理”时,若转移1mole-,则可回收7gLi
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①~⑩在表中的位置,用化学用语回答下列问题:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
1 | ① | |||||||
2 | ② | ③ | ④ | ⑤ | ||||
3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)在这些元素中,化学性质最不活泼的元素的原子结构示意图为___,形成的单质是半导体的是___(填元素名称)。
(2)⑥与⑨形成的化合物的电子式为___,①与②形成的最简单化合物的结构式为___。
(3
(4)气态氢化物最稳定的是___(填化学式),②、③、⑧的原子半径最小是__(填素符号)。
(5)④与⑧形成的化合物的属于___(填“离子化合物”或“共价化合物”),该晶体属于___晶体(填“离子”、“分子”、“原子”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com