
可逆反应:mA(s)+nB(g) qC(g),在一定温度的密闭容器中进行,B的体积分数(V(B)%)与压强的关系如图所示。下列叙述中正确的是( )
qC(g),在一定温度的密闭容器中进行,B的体积分数(V(B)%)与压强的关系如图所示。下列叙述中正确的是( )

A.m+n<q B.m+n>q C.n>q D.x点时,v(正)>v(逆)
科目:高中化学 来源: 题型:选择题
| A. | X单质在一定条件下能与Z的最高价氧化物发生置换反应 | |
| B. | 原子半径:Y>Z>W | |
| C. | 最高价氧化物对应水化物的酸性由弱到强的顺序:X<Z<W | |
| D. | 室温下,0.1mol/LW的气态氢化物的水溶液的pH=1 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上第一次月考化学卷(解析版) 题型:选择题
对于可逆反应 2AB3(g) A2(g)+3B2(g)(正反应为吸热),下列图象正确的是( )
A2(g)+3B2(g)(正反应为吸热),下列图象正确的是( )
A.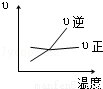 B.
B.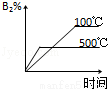 C.
C.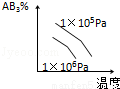 D.
D.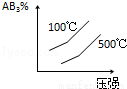
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上第一次月考化学卷(解析版) 题型:选择题
下列事实不能用勒夏特列原理来解释的是( )
A.往H2S水溶液中加碱有利于S2﹣增多
B.在二氧化硫的催化氧化反应中,通入过量的空气以提高二氧化硫的转化率
C.高压有利于合成NH3的反应
D.500℃左右比室温更有利于合成NH3的反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高一上10月阶段测化学卷(解析版) 题型:填空题
实验室常用盐酸的质量分数为36.5%,密度为1.20g/㎝3。
(1)此浓盐酸的物质的量浓度是 ?(列式计算)
(2)配制100mL3.00mol/L的盐酸,需以上浓盐酸 mL .(列式计算)
(3)还原4.8g金属氧化物,参加反应的氢气为2.016L(标准状况),生成的金属溶于上述盐酸,放出氢气1.344 L(标准状况),此金属氧化物是 。
A.Fe2O3 B.ZnO C.CuO
(4)将5.0 g CaC O3加入到足量的盐酸中,并将生成的气体全部通入足量的红热的碳中充分反应,可得到气体的体积为 。(折算成标况下)
O3加入到足量的盐酸中,并将生成的气体全部通入足量的红热的碳中充分反应,可得到气体的体积为 。(折算成标况下)
(5)某金属R与一定体积的上述盐酸正好完全反应所得氯化物溶液20 mL,浓度为0.05 mol/L。它恰好能与20 mL 0.15 mol·L-1 的AgNO3溶液完全反应,则该氯化物的化学式 .
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高一上10月阶段测化学卷(解析版) 题型:选择题
下列实验操作的描述中,正确的是 ( )
A. 取用Na2CO3溶液时,发现取量过多,为了不浪费,又把过量的试剂倒入试剂瓶中
B. 用溶解、过滤的方法分离氯化钠和硝酸钾的混合物
C. 称量NaOH固体,先在天平两盘上放大小相等纸片,然后NaOH放在左盘纸片上称量
D. 利用丁达尔效应可以区别溶液和胶体
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c(NH3)/mol•L-1 | 0.08 | 0.14 | 0.18 | 0.2 | 0.2 | 0.2 |
| 物质 | A | B | C | D |
| 起始投料/mol | 2 | 1 | 2 | 0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com