
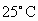 时,若体积为
时,若体积为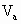 、
、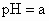 的某一元强酸与体积为
的某一元强酸与体积为 、pH=b的某一元强碱混合,恰好中和,且已知
、pH=b的某一元强碱混合,恰好中和,且已知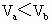 和a=0.5b.请填写下列空白:
和a=0.5b.请填写下列空白:
(1)a值可否等于3(填“可”或“否”)______________,其理由是____________________________.
(2)a值可否等于5(填“可”或“否”)___________________,其理由是____________________________.
(3)a的取值范围是多少?
科目:高中化学 来源: 题型:阅读理解
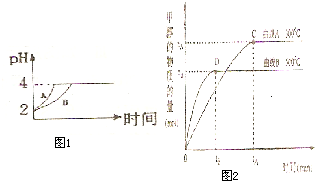 化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:
化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:| c(CH3OH) |
| c(CO)×c2(H2) |
| c(CH3OH) |
| c(CO)×c2(H2) |
| 2nB |
| 3tB |
| 2nB |
| 3tB |
查看答案和解析>>
科目:高中化学 来源: 题型:
| c(CO)?c(H2) | c(H2O) |

查看答案和解析>>
科目:高中化学 来源: 题型:
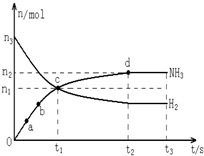 自1913年工业合成氨投产以来,合成氨工业不断发展,氨又可以进一步制备硝酸,在工业上可进行连续生产.请回答下列问题:
自1913年工业合成氨投产以来,合成氨工业不断发展,氨又可以进一步制备硝酸,在工业上可进行连续生产.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
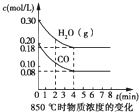 某研究小组利用反应CO(g)+H2O(g)?CO2(g)+2H2(g)△H=-41.2kJ/mol,制备CO2与H2的混合气体,并进一步研究CO2与H2以不同的体积之比混合时在合适条件下的反应情况.请回答下列问题:
某研究小组利用反应CO(g)+H2O(g)?CO2(g)+2H2(g)△H=-41.2kJ/mol,制备CO2与H2的混合气体,并进一步研究CO2与H2以不同的体积之比混合时在合适条件下的反应情况.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com