
下列电离方程式中书写正确的是
A.NaHSO4  Na++H++SO42- B.NaHCO3
Na++H++SO42- B.NaHCO3  Na++H++CO32-
Na++H++CO32-
C.HClO = H++ClO- D.H2S  H++HS-;HS-
H++HS-;HS-  H++S2-
H++S2-
科目:高中化学 来源: 题型:
原子序数由小到大排列的四种短周期元素X、Y、Z、W,四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族。M与X同主族,与W同周期。
(1)M元素是________(填元素符号)。
(2)Z、W形成的气态氢化物的稳定性为 > (填化学式)。
(3)M2Z2的电子式为________________,写出M2Z2与水反应的离子方程式:
。
(4)由X、Y、Z、W四种元素中的三种组成的—种强酸,该强酸的稀溶液能与铜反应,离子方程式为__________________________________________。
(5)由X、Y、Z、W四种元素组成的一种离子化合物A,已知:
①1 mol A能与足量NaOH浓溶液反应生成标准状况下44.8 L气体;
②A能与盐酸反应产生气体B,该气体能与氯水反应。
则A是____________(填化学式);写出该气体B与氯水反应的离子方程式:_______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
完全燃烧一定质量的无水乙醇,放出的热量为Q,为完全吸收生成的CO2,并使之生成正盐Na2CO3,消耗掉0.8mol/L NaOH溶液500mL,则燃烧1mol酒精放出的热量是( )
A.0.2Q B.0.1Q C.5Q D.10Q
查看答案和解析>>
科目:高中化学 来源: 题型:
对于平衡体系mA(气)+nB(气) PC(气)十qD(气) △H <0,有下列判断,其中正确的是
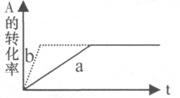 A.若温度不变,将容器的体积缩小1倍,此时A的浓度变为原来的1 .8倍,则m+n<p+q
A.若温度不变,将容器的体积缩小1倍,此时A的浓度变为原来的1 .8倍,则m+n<p+q
B.若平衡时,A、B的转化率相等,说明反应开始时A,B的物质的量之比为m:n
C.若平衡体系共有气体amol,再向其中加人bmolB,当重新达到平衡时,气体的总物质的量等于(a+b),则m+n>p+q
D.加催化剂或增大压强,可实现右图a→b的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,将0.1 mol·L-1NaOH溶液与0.06 mol·L-1 H2SO4溶液等体积混合,该混合溶液的pH等于
A.1.7 B.2.0 C.12.0 D.12.4
查看答案和解析>>
科目:高中化学 来源: 题型:
高温下,某反应达平衡,平衡常数K=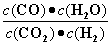 。恒容时,温度升高,H2浓度减小。下列说法正确的是
。恒容时,温度升高,H2浓度减小。下列说法正确的是
A.该反应的焓变为正值
B.恒温恒容下,增大压强,H2浓度一定减小
C.升高温度,逆反应速率减小
D.该反应化学方程式为CO+H2O CO2+H2
CO2+H2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于胶体的叙述不正确的是( )
A.胶体分散质颗粒的直径在1nm~100nm之间
B.向胶体中加入蔗糖溶液,产生聚沉现象
C.一束可见光透过胶体时,发生丁达尔现象
D.采用渗析的方法可以净化胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
乙酸苯甲酯( )广泛存在于可可、咖啡、草莓等物质中,可用作食物和日化用品的香精。已知:X的产量可以用来衡量一个国家的石油化工发展水平,工业上可用X和甲苯人工合成乙酸苯甲酯。其合成路线如下:
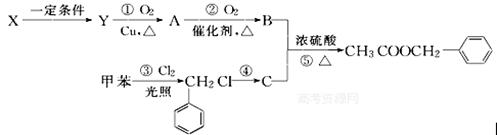
据此回答下列问题:
(1) 发生反应④的化学方程式为 ,该反应的反应类型为 。
(2)实验室为鉴别A和B两者的水溶液,可以选用的化学试剂是 。
A.纯碱溶液 B.NaOH溶液 C.金属钠 D.银氨溶液
(3)上述反应①~⑤中原子的理论利用率为100%、符合绿色化学要求的反应是______(填序号)。
(4)请写出反应⑤的化学方程式: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com