
废金属屑中主要成分为Cu、Fe和Al,此外还含有少量Al2O3和Fe2O3,该厂用上述废金属屑制取新型高效水处理剂Na2FeO4(高铁酸钠)等产品,过程如下:
Ⅰ.向废金属屑中加入过量的NaOH溶液,充分反应后过滤;
Ⅱ.向Ⅰ所得固体中加入过量稀H2SO4,充分反应后过滤;
Ⅲ.向Ⅱ所得固体中继续加入热的稀H2SO4,同时不断鼓入空气,固体溶解得CuSO4溶液;
Ⅳ.……
(1)步骤Ⅰ中发生反应的化学方程式为________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(2)步骤Ⅱ所得的滤液中加入KSCN溶液无明显现象,表明滤液中不存在Fe3+。用离子方程式解释其可能的原因________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(3)步骤Ⅲ获得CuSO4溶液的离子方程式为________________________________________________________________________
________________________________________________________________________。
(4)步骤Ⅱ所得滤液经进一步处理可制得Na2FeO4,流程如下:





①测得滤液中c(Fe2+)为a mol·L-1,若要处理滤液,理论上需要消耗25%的H2O2溶液 68a kg(用含a的代数式表示)。2-1-c-n-j-y
②写出由Fe(OH)3制取Na2FeO4的化学方程式 2Fe(OH)3+3NaClO+4NaOH 2Na2FeO4+3NaCl+5H2O 。
科目:高中化学 来源: 题型:
下列溶液一定呈中性的是 A.pH=7的溶液 B.c(H+)=c(OH-)=10-6mol/L的溶液
C.使石蕊试液呈紫色的溶液 D.酸与碱恰好完全反应生成正盐的溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中正确的是( )
A.干燥的Cl2和氯水均能使鲜花褪色
B.向碘水中通入SO2,碘水褪色说明SO2具有漂白性
C.向FeBr2溶液中滴加少量氯水,溶液变浅黄色是因为生成了Br2
D.将Cl2通入AgNO3溶液中不会有沉淀产生
查看答案和解析>>
科目:高中化学 来源: 题型:
硝酸是一种具有强氧化性的酸,它不仅能与活泼金属发生反应,也能与许多不活泼金属发生反应。其中金属铜与稀硝酸反应的化学方程式为3Cu+8HNO3(稀)===3Cu(NO3)2+2X↑+4H2O,则X的化学式为( )
A.NO2 B.NO
C.N2O D.N2O4
查看答案和解析>>
科目:高中化学 来源: 题型:
某校化学活动小组为探究X、Y、Z三种金属与酸的反应情况,进行了如下实验:等质量的X、Y、Z粉末分别与足量的溶质质量分数相同的稀硫酸反应,都生成+2价金属的硫酸盐,反应情况用下图来表示。下列顺序正确的是( )
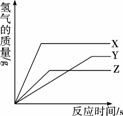
A.金属活动性由强到弱:X>Z>Y
B.金属活动性由强到弱:X>Y>Z
C.相对原子质量由大到小:X>Z>Y
D.相对原子质量由大到小:X>Y>Z
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于铝的叙述中正确的是( )
A.铝合金是一种混合物,它比纯铝的熔点高
B.由于铝的导电性比铜、银都强,所以常用其制造电线、电缆
C.由于铝具有强还原性,所以可以通过铝热反应冶炼某些高熔点金属
D.常温下,由于铝与浓硫酸钝化时不反应,所以可用铝制槽车运送浓硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
向某晶体的水溶液中加入FeCl2的溶液后,无明显变化,当滴加几滴溴水后,混合液出现血红色。那么,由此得出的下列结论错误的是( )21教育名师原创作品
A.该晶体中一定含有SCN-
B.Fe3+与SCN-形成了血红色Fe(SCN)3难溶物
C.Fe2+被Br2氧化为Fe3+
D.Fe2+与SCN-不能形成血红色物质
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:(1)Zn(s)+1/2O2(g)===ZnO(s) ΔH=-348.3 kJ·mol-1
(2)2Ag(s)+1/2O2(g)===Ag2O(s) ΔH=-31.0 kJ·mol-1
则Zn(s)+Ag2O(s)===ZnO(s)+2Ag(s)的ΔH等于
A.-317.3 kJ·mol-1 B.-379.3 kJ·mol-1
C.-332.8 kJ·mol-1 D.317.3 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
某物质的分子式为CxHyOz,取该物质ag在足量的O2中充分燃烧后,将产物全部通入过量的Na2O2中,若Na2O2固体的质量增加了bg,并且a<b,则x、y、z必须满足的关系是( )
A.x>z B.x=y=z C.x=z D.x<z
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com