
分析 (1)碱式碳酸钠铝[NaaAlb(OH)c(CO3)d]中,化合价代数和为0;
(2)碱式碳酸钠铝作为阻燃剂的可能原因:①在分解过程中大量吸热;②本身及产物无毒且不可燃;③同产生不支持燃烧的二氧化碳和水;
(3)pH过高,碱性强不生成氢氧化铝,而产生偏铝酸盐;
(4)因为:n(CO2)=$\frac{0.448L}{22.4L/mol}=0.02mol$,n(CO2)=0.02mol,所以n(H2O)=$\frac{2.880g×(1-56.9%)-0.02mol×44g/mol}{18g/mol}=0.02mol$,而测得溶液中含有0.02molAl3+,所以b:c:d=1:2:1,根据电荷守恒a+0.02×3=0.02×2+0.02×2,所以a=0.02mol,所以a:b:c:d=1:1:2:1,由此分析解答.
解答 解:(1)碱式碳酸钠铝[NaaAlb(OH)c(CO3)d]中,化合价代数和为0,所以a+3b-c-2d=0,则a+3b=c+2d,故答案为:a+3b=c+2d;
(2)碱式碳酸钠铝作为阻燃剂的可能原因:①在分解过程中大量吸热;②本身及产物无毒且不可燃;③同产生不支持燃烧的二氧化碳和水,故答案为:产生阻燃性气体CO2、H2O;
(3)pH过高,碱性强不生成氢氧化铝,而产生偏铝酸盐,所以pH过高,则对产品的影响是会使碱式碳酸钠铝转化为NaAlO2,故答案为:pH过高会使碱式碳酸钠铝转化为NaAlO2;
(4)因为:n(CO2)=$\frac{0.448L}{22.4L/mol}=0.02mol$,n(CO2)=0.02mol,所以n(H2O)=$\frac{2.880g×(1-56.9%)-0.02mol×44g/mol}{18g/mol}=0.02mol$,而测得溶液中含有0.02molAl3+,所以b:c:d=1:2:1,根据电荷守恒a+0.02×3=0.02×2+0.02×2,所以a=0.02mol,所以a:b:c:d=1:1:2:1,所以,碱式碳酸铝的化学组成为NaAl(OH)2CO3,故答案为:NaAl(OH)2CO3.
点评 本题考查化学方程式有关计算,为高频考点,明确各个物理量之间关系是解本题关键,注意原子守恒的灵活运用,题目难度不大.


 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源: 题型:解答题
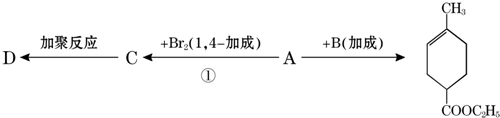
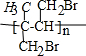 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化镁的熔点高,可用作耐火材料 | |
| B. | 碳酸钠具有弱碱性,可用作胃酸中和剂 | |
| C. | 二氧化硫具有漂白性,可用作漂白纸浆 | |
| D. | 氯化铁溶液能腐蚀铜,可用于制作印刷电路板 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,pH=8的碱性溶液中不可能存在H2CO3分子 | |
| B. | 常温下,pH均为5的盐酸与氯化铵溶液中,水的电离程度相同 | |
| C. | 0.1mol/LCH3COOH溶液加水稀释,溶液的pH和CH3COOH的电离度均增大 | |
| D. | 将BaCl2溶液滴入含酚酞的Na2CO3溶液,红色褪去,说明BaCl2溶液显酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7.8g苯中碳碳双键的数目为0.3NA | |
| B. | 由1mol CH3COONa和少量CH3COOH形成的中性溶液中,CH3COO-的个数为NA | |
| C. | 常温常压,11.2L NO和O2混合气体的原子数为NA | |
| D. | 50mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子数为0.46NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
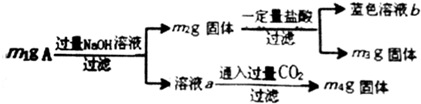
| A. | 由m1、m2、m4可计算出混合物中Al、Al2O3的物质的量 | |
| B. | 生成蓝色溶液的离子方程式为Cu+2Fe3+=Cu2++2Fe2+ | |
| C. | 蓝色溶液中一定有Cu2+、Fe2+、Fe3+ | |
| D. | 当m2-m3=2.96g时,Fe3O4的质量至少为2.32g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
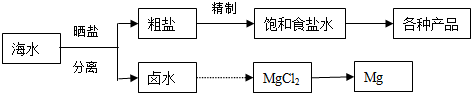
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入氢氧化钠固体 | B. | 加水 | ||
| C. | 通入二氧化碳气体 | D. | 加入饱和石灰水溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com