
���� ��1����Ԫ��ԭ������Ϊ7�����ݹ���ԭ��������K������L�㣬K��2�����ӣ�L��Ϊ5�����ӣ����ǹ��ۻ����ﵪԭ�Ӻ���ԭ���γɹ��ۼ�����ԭ�Ӻ͵�ԭ�Ӽ�Ҳ�γɹ��ۼ���
��2�����ݸ�˹���ɣ��ڡ�2-�ٵõ���2N2H4��l��++N2O4��l��=3N2��g��+4H2O��g������Ӧ���뻯ѧ�����������ȣ�
��3��ȼ������ָ1mol��ȼ����ȫȼ�������ȶ���������ʱ���ų�������������ȼ���ȵĸ����ϸ�˹���ɽ��
��� �⣺��1����Ԫ��ԭ������Ϊ7�����ݹ���ԭ��������K������L�㣬K��2�����ӣ�L��Ϊ5�����ӣ����ǹ��ۻ����ﵪԭ�Ӻ���ԭ���γɹ��ۼ�����ԭ�Ӻ͵�ԭ�Ӽ�Ҳ�γɹ��ۼ����ṹʽΪ��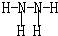 ��
��
�ʴ�Ϊ��5�����ۼ���
��2������N2��g��+2O2��g��=N2O4��l����H1=-19.5kJ?mol-1
��N2H4��l��+O2 ��g��=N2��g��+2H2O��g����H2=-534.2kJ•mol-1
���ݸ�˹����д���º�N2O4��Ӧ���Ȼ�ѧ���̣��ڡ�2-�ٵõ���2N2H4��l��++N2O4��l��=3N2��g��+4H2O��g����H=��-534.2����2-��-19.5��kJ•mol-1=-1048.9 kJ•mol-1��
�ʴ�Ϊ��2N2H4��l��+N2O4��l��=3N2��g��+4H2O��g����H=-1048.9 kJ•mol-1��
��3��ȼ���ȣ�ָ���ɵ�ˮ����ΪҺ̬����ȼ�����Ϊ1mol��
�ɷ�Ӧ��N2H4��l��+O2 ��g��=N2��g��+2H2O��g����H2=-534.2kJ•mol-1
��H2O��l���TH2O��g����H3=+44kJ•mol-1
����-2���ڿɵã�N2H4��l��+O2 ��g��=N2��g��+2H2O��l����H2=-622.2kJ•mol-1
�ʴ�Ϊ��N2H4��l��+O2 ��g��=N2��g��+2H2O��l����H2=-622.2kJ•mol-1��
���� ���⿼����ԭ�Ӻ�������Ų����µĻ�ѧ�����Ȼ�ѧ����ʽ����˹���ɵ�Ӧ�õ�֪ʶ��ע���˹���ɵ�����Ӧ�ã�Ϊ��Ƶ���㣬��Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaH��ˮ���Լ��� | |
| B�� | NaH����Ԫ�ص����ӵĵ��Ӳ��Ų�����ԭ�ӵĵ��Ӳ��Ų���ͬ | |
| C�� | ���뾶H-��Li+ | |
| D�� | NaH��H2O��Ӧʱ��ˮ����ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| ��ʵ�鷽�� | ʵ������ |
| ����ɰֽ��ĥ���þ�����ˮ��Ӧ������ӦҺ�еμӷ�̪ | �������壬�����ȼ����Һ��dz��ɫ |
| �������Ƶ�Na2S������Һ�еμ�������ˮ | ���ɵ���ɫ���� |
| ��������з�̪��Һ����ˮ��Ӧ | ����ˮ���ϣ��۳�С���Ĵ��ζ�������С����Һ���ɫ |
| ��þ����2mol/L�����ᷴӦ | ���ҷ�Ӧ�������������ȼ |
| ��������2mol/L�����ᷴӦ | ��Ӧ��ʮ�־��ң������������ȼ |
| ����AlCl3��Һ�еμ�NaOH��Һ������ | �����ɰ�ɫ��״������������ȫ���ܽ� |
| ʵ�鷽�� | ʵ������ | �й����ӷ���ʽ |
| �� | ���� | ���� |
| �� | S2-+Cl2=S��+2Cl- | |
| �� | ���� | 2Na+2H2O=2Na++2OH-+H2�� |
| �� | ���� | ���� |
| �� | ���� | 2Al+6H+=2Al3++3H2�� |
| �� | �����ɰ�ɫ��״������������ȫ���ܽ� | Al3++3OH-=Al��OH��3����Al��OH��3+OH-=AlO2-+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HA��ǿ�� | |
| B�� | ���Һ�У�c��HA��+c��A-��=0.4mol•L-1 | |
| C�� | ���Һ�У�c��Na+��+c��H+��=$\frac{Ka��HA��•c��HA��+Kw}{c��{H}^{+}��}$ | |
| D�� | ����Һ�м�������ˮ��c��A-����c��HA���ı�ֵ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
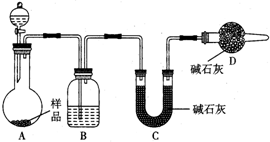 Ϊ�ⶨ�����Ѿõ�С�մ���Ʒ�д���������������������ʵ�鷽����
Ϊ�ⶨ�����Ѿõ�С�մ���Ʒ�д���������������������ʵ�鷽�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��ѧ�� | H-H | N��N |
| ����/kJ•mol-1 | 435 | 943 |

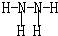 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2�� | B�� | 3�� | C�� | 4�� | D�� | 5�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com