
| A. | 11.2LCO和N2混合气体中含有的分子数是0.5NA | |
| B. | 在氯气参与的反应中,22.4L(标况)氯气完全反应得到的电子数一定为0.2NA | |
| C. | 1 mol SO2与足量O2在一定条件下反应生成SO3,共转移2NA个电子 | |
| D. | l L l mol•L-1的NaClO溶液中含有ClO-的数目小于NA |
分析 A、气体所处的状态不明确;
B、氯气参与反应时不一定得电子,还可能失电子或发生歧化反应;
C、二氧化硫和氧气的反应为歧化反应;
D、次氯酸根为弱酸根,在溶液中会水解.
解答 解:A、没有指明是标准状况,无法根据气体的体积计算物质的量,故A错误;
B、Cl2与H2O或NaOH等强碱反应,Cl2既是氧化剂也是还原剂,22.4L(标况)氯气物质的量为1mol,得电子数为NA,故B错误;
C、SO2与O2的反应是可逆反应,1mol SO2不可能全部反应,所以1 mol SO2与足量O2在一定条件下反应生成SO3,共转移电子数小于2NA,故C错误;
D、NaClO为弱酸强碱盐,ClO?发生水解反应,所以l L l mol/L的NaClO溶液中含有ClO-的数目小于NA,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:实验题
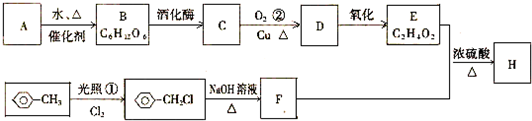
 ,
,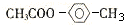 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷的燃烧热为-890.3 kJ•mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | S(g)+O2(g)═SO2(g)△H1 S(s)+O2(g)═SO2(g)△H2则△H1<△H2 | |
| C. | 已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定 | |
| D. | 已知中和热为△H=-57.3kJ•mol-1,则稀醋酸和稀NaOH溶液反应的热化学方程式为:CH3COOH(aq)+NaOH(aq)═CH3COONa(aq)+H2O(l)△H=-57.3 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 漂白粉溶液在空气中失效:ClO-+CO2+H2O═HClO+HCO3- | |
| B. | 用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O | |
| C. | 向NaAlO2溶液中通入过量CO2制Al(OH)3:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3- | |
| D. | 碳酸钙与醋酸溶液反应:CaCO3+2H+═Ca2++CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该物质中含有三种金属元素 | |
| B. | 该物质的一个分子中含有10个原子 | |
| C. | 该物质由四种原子直接构成 | |
| D. | 该物质中钠元素与氧元素质量比为1:6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 编号 | 1 | 2 | 3 |
| 加3%Na2S2O3溶液 | 5mL | 5mL | 5mL |
| 1:5的硫酸 | 25滴 | 15滴 | 25滴 |
| 温度/℃ | 室温 | 室温+10 | 室温+20 |
| 出现浑浊的快慢 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com