
常温下,有下列四种溶液:①pH=2的CH3COOH溶液;②pH=2的HCl溶液;③pH=12的氨水;④pH=12的NaOH溶液。下列有关说法正确的是
A.四种溶液的KW相同,由水电离的c(H+):①=③>②=④
B.向等体积的四种溶液中分别加入100 mL水后,溶液的pH:③>④>②>①
C.①、②、④溶液分别与足量铝粉反应,生成H2的量:②最大
D.将②、③两种溶液混合后,若pH=7,消耗溶液的体积为:③>②
B
【解析】
试题分析:A.相同条件下,水的离子积常数是定值,无论酸还是碱都抑制水的电离,①pH=2的CH3COOH溶液;②pH=2的HCl溶液;③pH=12的氨水;④pH=12的NaOH溶液,①、②的氢离子浓度相同,③、④的氢氧根离子的浓度相同,所以这四种溶液中由水电离的C(H+):①=②=③=④,错误;
B.醋酸是弱酸,加水稀释后能促进醋酸的电离,所以①、②稀释后溶液的PH值7>②>①;氨水是弱碱,加水稀释后能促进氨水的电离,所以③、④、稀释后溶液的PH值③>④>7,所以向等体积的四种溶液中分别加入100mL水后,溶液的pH:③>④>②>①,正确;
C.醋酸是弱酸,氯化氢和氢氧化钠是强电解质,①、②、④三种溶液的物质的量浓度关系为:①>②=④,所以等体积的①、②、④溶液分别与铝粉反应,生成H2的量:②、④一样多,错误;
D.pH=12的氨水只有部分电离,所以C(NH3.H2O)>C(OH-),HCl是强电解质,所以其溶液中C(HCl)=C(H+),C(NH3.H2O)>C(HCl),若将NH3.H2O和HCl混合后溶液呈中性,则消耗溶液的体积:②>③,错误;
考点: 溶液pH的定义;弱电解质在水溶液中的电离平衡。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2014-2015学年山东省莱芜市高三1月月考化学试卷(解析版) 题型:实验题
(13分)实验室为探究铁与浓硫酸的反应,并验证SO2的性质,设计如图所示装置进行实验。

请回答下列问题:
(1)实验时A中导管a插入浓硫酸中,可使B中的溶液不发生倒吸。其原因是_______。
(2)B中酸性KMnO4逐渐褪色,则B中反应的离子方程式是_______________________;C中反应的化学方程式是_________________。
(3)D装置的作用是________;实验结束时需从a导管通入大量空气,其目的是___________。
(4)欲探究A装置中反应后铁元素的价态,设计实验方案如下:将反应后试管中的溶液稀释。取少许溶液,滴入3~5滴________溶液,若溶液呈红色,则证明含有Fe3+,否则不含Fe3+;取少许溶液,滴入3~5滴________溶液,若溶液褪色,则证明含有Fe2+,否则不含Fe2+。若实验证明反应后的溶液中只含有Fe3+,则A中反应的化学方程式是___________________________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省菏泽市高三1月月考化学试卷(解析版) 题型:选择题
两个装置中,液体体积均为200 mL,开始工作前电解质溶液的浓度均为0.5 mol/L,工作一段时间后,测得有0.02 mol电子通过,若忽略溶液体积的变化,下列叙述正确的是

A.产生气体体积 ①=②
B.①中阴极质量增加,②中正极质量减小
C.电极反应式:①中阳极:4OH- - 4e- →2H2O+O2↑②中负极:2H++2e-→H2↑
D.溶液的pH变化:①减小,②增大
查看答案和解析>>
科目:高中化学 来源:2014-2015陕西省西安市高二上学期期末化学试卷(解析版) 题型:实验题
(8分)某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中。
②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数。
③向锥形瓶中滴入酚酞作指示剂,进行滴定。滴定至指示剂刚好变色,且并不马上变色为止,测得所耗盐酸的体积为V1mL。
④重复以上过程,但在滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL。试回答下列问题:
(1)锥形瓶中的溶液从 色变为 色时,停止滴定。
(2)滴定时边滴边摇动锥形瓶,眼睛应观察
A、滴定管内液面的变化
B、锥形瓶内溶液颜色的变化
(3)该小组在步骤①中的错误是 由此造成的测定结果 (偏高、偏低或无影响)
(4)步骤②缺少的操作是
(5)下图,是某次滴定时的滴定管中的液面,其读数为 mL
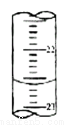
(6)根据下列数据:
滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
滴定前读数(mL) | 滴定后读数(mL) | ||
第一次 | 25.00 | 0.50 | 20.40 |
第二次 | 25.00 | 4.00 | 24.10 |
请计算待测烧碱溶液的浓度(保留四位小数) mol/L
查看答案和解析>>
科目:高中化学 来源:2014-2015陕西省西安市高二上学期期末化学试卷(解析版) 题型:选择题
下列各组离子在指定条件下,一定能大量共存的是
A.使石蕊试液变红色的溶液中:K+、Na+、CO32-、NO3-
B.在酸性高锰酸钾溶液中:Na+、NH4+、I-、Br-
C.c(H+)=10-1 mol/L的溶液中:Cu2+、Al3+、SO42-、NO3-
D.水电离出的c(H+)=10-12 mol/L的溶液中:Na+、Mg2+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源:2014-2015陕西省西安市高二上学期期末化学试卷(解析版) 题型:选择题
已知:HCN( aq)与NaOH(aq)反应的ΔH=-12.1 kJ·mol-1; HCl(aq)与NaOH(aq)反应的ΔH=-55. 6 kJ·mol-1。则HCN在水溶液中电离的ΔH等于
A.-67.7 kJ·mol-1 B.-43.5 kJ·mol-1
C.+43.5 kJ·mol-1 D.+67.7 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2014-2015陕西省西安市高二上学期期末化学试卷(解析版) 题型:选择题
在四个不同的容器中,在不同条件下进行合成氨的反应。根据下列在相同时间内测定的结果判断,生成氨的速率最快的是
A.v(H2)=0.1 mol·L-1·min-1
B.v(N2)=0.1 mol·L-1·min-1
C.v(N2)=0.2 mol·L-1·min-1
D.v(NH3)=0.3 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏徐州市高一上学期期末考试化学试卷(解析版) 题型:选择题
现有三种液态混合物:①乙酸(沸点118℃)和乙酸乙酯(沸点77.1℃);②汽油和水;③溴水。在实验室分离这三种混合物的正确方法依次为
A.蒸馏、分液、萃取 B.萃取、蒸馏、分液
C.分液、蒸馏、萃取 D.蒸馏、萃取、分液
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省浏阳市高二上学期理科化学试卷(解析版) 题型:选择题
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是
A.放电时负极反应为:Zn-2e-+2OH-=Zn(OH)2
B.充电时阳极反应为:Fe(OH)3-3e-+5OH-=FeO42-+4H2O
C.放电时每转移3mol电子,正极有1mol K2FeO4被氧化
D.放电时正极附近溶液的碱性增强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com