
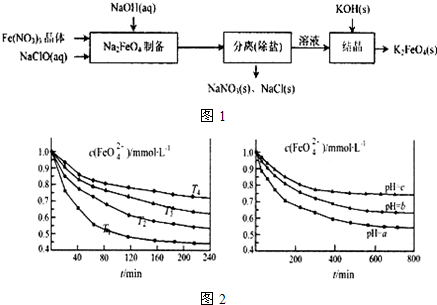
分析 (1)Fe3+可水解生成Fe(OH)3胶体,氢氧化铁胶体具有吸附作用;
(2)①2FeSO4+6Na2O2═2Na2FeO4+2Na2O+2Na2SO4+O2↑,6molNa2O2中12mol的负一价氧,2mol的有变成0价,还有10mol变成-2价,而铁是正2价变为正6价,所以每生成2mol Na2FeO4时转移电子10mol;
②Fe(NO3)3被NaClO氧化成Na2FeO4;结晶过程中钾离子和高铁酸根离子反应生成高铁酸钾沉淀;
(3)①温度越高,相同时间内FeO42-浓度变化越快,高铁酸钾溶液平衡时FeO42-浓度越小;温度越高FeO42-浓度越小,正向反应是吸热反应;
②pH越小,氢离子浓度越大,然后根据平衡移动解题.
解答 解:(1)Fe3+可水解水解的方程式为Fe3++3H2O?Fe(OH)3(胶体)+3H+,生成具有吸附性的Fe(OH)3胶体,能吸附悬浮在水中的杂质净水,发生聚沉;
故答案为:聚沉;
(2)①2FeSO4+6Na2O2═2Na2FeO4+2Na2O+2Na2SO4+O2↑,6molNa2O2中12mol的负一价氧,2mol的有变成0价,还有10mol变成-2价,而铁是正2价变为正6价,所以每生成2mol Na2FeO4时转移电子10mol,
故答案为:10;
②Fe(NO3)3被NaClO氧化成Na2FeO4,其反应的化学方程式为:2Fe(NO3)3+3NaClO+10NaOH=2Na2FeO4+3NaCl+6NaNO3+5H2O;结晶过程中反应的离子方程式为2K++FeO42-=K2FeO4↓,
故答案为:2Fe(NO3)3+3NaClO+10NaOH=2Na2FeO4+3NaCl+6NaNO3+5H2O;2K++FeO42-=K2FeO4↓;
(3)①由图1数据可知,温度越高,相同时间内FeO42-浓度变化越快,高铁酸钾溶液平衡时FeO42-浓度越小,温度越高FeO42-浓度越小,所以K2FeO4的稳定性随着温度的升高而减弱,
故答案为:K2FeO4的稳定性随着温度的升高而减弱;
②pH越小,氢离子浓度越大,由4FeO42-+10H2O=4Fe(OH)3(胶体)+8OH-+3O2↑可知:氢离子浓度增大,平衡向正反应方向移动,高铁酸钾溶液平衡时FeO42-浓度越小,pH越小,由图知a<c,
故答案为:<;由4FeO42-+10H2O=4Fe(OH)3(胶体)+8OH-+3O2↑可知:氢离子浓度增大,平衡向正反应方向移动,高铁酸钾溶液平衡时FeO42-浓度越小,pH越小.
点评 本题考查学生阅读题目获取信息的能力、铁的化合物的性质、氧化还原反应、化学平衡移动等,题目难度中等,要求学生要有扎实的基础知识和灵活运用知识解决问题的能力,注意基础知识的全面掌握.


科目:高中化学 来源: 题型:选择题
| A. | 反应(1)中x=6 | |
| B. | 反应(2)中的氧化产物与氧化剂的物质的量之比为4:5 | |
| C. | 反应(3)中的氧化剂是S,还原剂是KOH | |
| D. | NaClO3、NO、H2O、KOH、K2SO3中均含氧元素,但它们不全为氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁和硫酸铜溶液反应得到铜 | |
| B. | 铁和稀盐酸反应生成H2和FeCl2 | |
| C. | 铁高温下和水蒸气反应生成H2和Fe2O3 | |
| D. | 铁在氧气中燃烧生成Fe3O4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
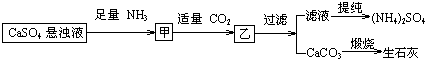
| A. | 通入CO2和NH3顺序可以颠倒 | |
| B. | 通入的NH3必须过量 | |
| C. | CO2可被循环使用 | |
| D. | 生成1mol(NH4)2SO4至少消耗2 mol NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| T/K | T1 | T2 | T3 |
| K | 1.00×107 | 2.54×105 | 1.88×103 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
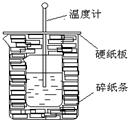 50ml0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中放出的热量可计算中和热.回答下列问题:
50ml0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中放出的热量可计算中和热.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com