
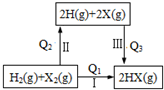
| A. | Q3>0 | B. | Q1=Q2+Q3 | ||
| C. | 按Cl、Br、I的顺序,Q2依次增大 | D. | Q1越大,HX越稳定 |
分析 A.原子形成化学键放热,则Q3大于0;
B.依据盖斯定律分析,反应焓变与起始物质和终了物质有关于变化途径无关;
C.途径Ⅱ是断裂化学键的过程,是吸热过程,Cl、Br、I的原子半径依次增大,Cl2、Br2、I2,断裂化学键需要能量减小;
D.反应中放热热量越多,形成的化合物具有的能量越小,则形成物质越稳定.
解答 解:A.原子形成化学键过程中放热,则反应2H(g)+2X(g)═2HX(g)的Q3>0,故A正确;
B.根据盖斯定律可知,途径Ⅰ生成HX的反应热与途径无关,所以Q1=Q2+Q3 ,故B正确;
C.Cl、Br、I的原子半径依次增大,Cl2、Br2、I2断裂化学键需要能量减小,所以途径Ⅱ按Cl、Br、I的顺序,吸收的热量Q2依次减小,故C错误;
D.Q1为氢气和卤素单质形成HX的过程,该反应中Q1越大,说明放出的热量越多,则生成的HX具有能量越低,HX越稳定,故D正确;
故选C.
点评 本题考查了化学反应中的能量变化、盖斯定律的应用,题目难度中等,明确化学反应与能量不会的关系为解答关键,注意掌握盖斯定律的含义及应用方法,试题培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 16g CH4与18g NH4+所含的质子数为10NA | |
| B. | 将15.6g Na2O2投入到足量水中,反应后溶液中的氧原子数为0.4NA | |
| C. | 在1L 0.1mol•L-1的碳酸钠溶液中,阴离子总数一定大于0.1NA | |
| D. | 2mol NO和1mol O2混合,所得气体的分子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | x=5 | |
| B. | 每生成16 mol N2转移10 mol电子 | |
| C. | N2既是氧化产物又是还原产物 | |
| D. | 反应中氧化产物与还原产物的质量之比为1:15 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 地球上99%以上的溴蕴藏在海洋中 | |
| B. | 用食醋可除去热水壶内壁的水垢 | |
| C. | 在水库铁闸门上接装铜块可减缓铁闸门腐蚀 | |
| D. | 将煤气化或液化可减少污染、提高燃烧效率 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 该物质为离子晶体 | |
| B. | 该物质可用通过C60吸附N2而制得 | |
| C. | C(N3)4中碳元素为正价 | |
| D. | 18g该物质完全分解可以产生13.44升(标准状况)氮气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8g | B. | 0.8g | C. | 1.6g | D. | 16g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com