
Na2CO3����ȡ������Na2CO3��NaHCO3�ۺ�ʵ��̽��
�� (1)�ҹ���ѧ�Һ�°�ĸ����Ĵ����������գ����������̿ɼ�Ҫ��ʾ����:
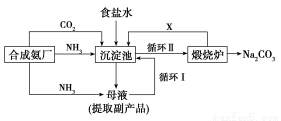
��������ʳ��ˮ������ͨ��������NH3��CO2(���)��������ͨCO2��ͨNH3��ԭ����_______________________________________________��
��д���������з�Ӧ�Ļ�ѧ����ʽ_______________________________________________��
��ijʵ��С��̽��Na2CO3��NaHCO3�����ʣ�����ʵ������ʢ�����ֹ�����Լ�ƿ��ʧ�˱�ǩ�����ǣ������ȶԹ���A��B���м�����ͨ��ʵ���������̽����
(2)�ֱ���ȹ���A��B�����ֹ���A���Ȳ�����������ʹ����ʯ��ˮ����ǡ�A���ȷֽ�Ļ�ѧ����ʽΪ_______________________________________________��
(3)��ȡ���ֹ����2 g���ֱ��������С�ձ��У��ٸ���10 mL����ˮ���������¶ȱ仯�����������ܽ⣬�ָ������£���������Һ�и�����2�η�̪��Һ��
�ٷ���Na2CO3������ȫ�ܽ⣬��NaHCO3������ʣ�࣬�ɴ˵ó����ۣ�_______________________��
��ͬѧ�������ձ��л��۲쵽�����������У�ʢ��Na2CO3���ձ��г��ֵ�������________(����ĸ���)��
a����Һ�¶��½�
b����Һ�¶�����
c�������̪���dz��ɫ
d�������̪��ʺ�ɫ
(4)ͬѧ�ǽ����ֹ���ֱ����Ƴ�0.5 mol��L��1����Һ��������·������Է�Ӧ��������Ԥ�⣺
ʵ�鷽�� | Ԥ������ | Ԥ������ |
����1����2 mL Na2CO3��Һ�еμ�1 mL 0.5 mol��L��1 CaCl2��Һ | �а�ɫ���� | Na2CO3��Һ�е�COŨ�Ƚϴ�����CaCl2������Ӧ��Ca2����CO===CaCO3�� (���ӷ���ʽ) |
����2����2 mL NaHCO3��Һ�еμ�1 mL 0.5 mol��L��1 CaCl2��Һ | �ް�ɫ���� | NaHCO3��Һ�е�COŨ�Ⱥ�С��������CaCl2��Ӧ |
ʵʩʵ����ֲ���2��������Ԥ���в��죺������ɫ���������壬��������£�NaHCO3��Һ��CaCl2��Һ��Ӧ�����ӷ���ʽΪ________________��
 �ִʾ��ƪϵ�д�
�ִʾ��ƪϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ɹŸ�һ����ĩ����ѧ�������棩 ���ͣ�ѡ����
�����йز�����ȷ���ǣ� ��
A. FeBr3��������������ˮ������Ӧ��������ɫ����ˮ�ص�Һ���屽
B. �������ữ�ĸ��������Һ������ױ�
C. ��ͭ˿�������״���ھƾ����ϼ��ȱ�ں���������ʢ����ˮ�Ҵ����Թ��У�ʵ���Ҵ�������Ϊ��ȩ��ʵ��
D. ������ˮ�������������Ҵ������Ȼ�̼�����л���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����������и�һ����ĩ���Ի�ѧ���������棩 ���ͣ������
�״���һ����Ҫ�Ļ���ԭ�Ϻ�����ȼ�ϡ�
(1)��ҵ��һ����CO��H2Ϊԭ�����ܱ������кϳɼ״���CO(g)��2H2(g) CH3OH(g)����H����90.8 kJ��mol��1�����ݻ�Ϊ1 L�ĺ��������У��ֱ��о���230 �桢250 ���270 �������¶��ºϳɼ״��Ĺ��ɡ���ͼ�����������¶���H2��CO����ʼ��ɱ�(��ʼʱCO�����ʵ�����Ϊ1 mol)��COƽ��ת���ʵĹ�ϵ��������Z��Ӧ���¶���________�����¶���������Ӧ�Ļ�ѧƽ�ⳣ��Ϊ________��
CH3OH(g)����H����90.8 kJ��mol��1�����ݻ�Ϊ1 L�ĺ��������У��ֱ��о���230 �桢250 ���270 �������¶��ºϳɼ״��Ĺ��ɡ���ͼ�����������¶���H2��CO����ʼ��ɱ�(��ʼʱCO�����ʵ�����Ϊ1 mol)��COƽ��ת���ʵĹ�ϵ��������Z��Ӧ���¶���________�����¶���������Ӧ�Ļ�ѧƽ�ⳣ��Ϊ________��

(2)��ͼ�Ǽ״�ȼ�ϵ�ع�����ʾ��ͼ������A��B��D��Ϊʯī�缫��CΪͭ�缫������һ��ʱ��Ͽ�K����ʱA��B�����ϲ��������������ͬ��

I.���и����ĵ缫��ӦʽΪ_________ _______
II�����з�Ӧ�Ļ�ѧ����ʽΪ______ __ ________��A�������������ڱ�״���µ����Ϊ________________��
III����װ����Һ�н��������ӵ����ʵ�����ת�Ƶ��ӵ����ʵ����仯��ϵ����ͼ����ͼ�Т��߱�ʾ����________�ı仯����Ӧ������Ҫʹ��װ���н���������ǡ����ȫ��������Ҫ________ mL 5.0 mol��L��1 NaOH��Һ��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����������и�һ����ĩ���Ի�ѧ���������棩 ���ͣ�ѡ����
ij��Ԫ��(H2A)��ˮ�еĵ��뷽��ʽΪH2A===H����HA����HA�� H����A2��(25 ��ʱKa��1.0��10��2)�������й�˵������ȷ����(����)
H����A2��(25 ��ʱKa��1.0��10��2)�������й�˵������ȷ����(����)
A��H2A������
B��ϡ��0.1 mol/L H2A��Һ�������ƽ�������ƶ�������c(H��)����
C����0.1 mol/L��H2A��Һ�У�c(H��)��0.12 mol/L
D����0.1 mol/L NaHA��Һ��c(H��)��0.02 mol/L����0.1 mol/L��H2A��c(H��)<0.12 mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����������и�һ����ĩ���Ի�ѧ���������棩 ���ͣ�ѡ����
��ʢ��NH4HCO3��ĩ��С�ձ�����ʢ����������Ĵ��ձ��С�Ȼ����С�ձ��м������ᣬ��Ӧ���ң����������̡��ɴ˿ɼ� (����)
A��NH4HCO3������ķ�Ӧ�Ƿ��ȷ�Ӧ
B���÷�Ӧ�У�����ת��Ϊ�����ڲ�������
C����Ӧ��������������������������
D����Ӧ���Ȼ�ѧ����ʽΪNH4HCO3��HCl��NH4Cl��CO2����H2O����H����Q kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����������и߶�����ĩ����ѧ���������棩 ���ͣ�ѡ����
����������һ����Ҫ�Ļ���ԭ�ϣ������Ʊ�һϵ������(��ͼ��ʾ)������˵���������(����)

A����ʽ������ˮ���ܲ���Fe(OH)3���壬��������ˮ��
B��Ϊ��ֹNH4HCO3�ֽ⣬����FeCO3���ڽϵ��¶��½���
C������KSCN��Һ����(NH4)2Fe(SO4)2�Ƿ�����
D�������£�(NH4)2Fe(SO4)2��ˮ�е��ܽ�ȱ�FeSO4�Ĵ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����������и߶�����ĩ����ѧ���������棩 ���ͣ�ѡ����
������60%��þ�ǴӺ�ˮ����ȡ�ģ�����Ҫ�������£�
�ٰѱ����Ƴ���ʯ�ң����ں�ˮ�м�����ʯ�ң����ˡ�ϴ�ӳ�����۽������������ᷴӦ���ᾧ�����ˣ������Ȼ����������м��Ⱦ��壻�ݵ������������(����������)������˵����ȷ����(����)
A����ϴ��Һ�еμ��Ȼ�����Һ�ɼ�������Ƿ�ϴ�Ӹɾ�
B�������仯�����а����˷ֽ⡢���ϡ����ֽ⡢�û������ַ�Ӧ����
C����������Ȼ����������м��Ⱦ����Ŀ����Ϊ�˷�ֹ�Ȼ�þˮ��
D�������Ҳ���Բ��õ�����ˮ��Һ�ķ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꼪�ֳ�����ʮһ���и߶�����ĩ���Ի�ѧ���������棩 ���ͣ�ѡ����
���з�Ӧ�����ӷ���ʽ��ȷ���ǣ�������
A��̼�������Һ�ӵ������У�Ca(HCO3)2+2CH3COOH Ca2��+2CH3COO��+2CO2��+2H2O
Ca2��+2CH3COO��+2CO2��+2H2O
B����AgNO3��Һ�еμӹ�����ˮ��Ag��+ NH3��H2O AgOH��+NH4��
AgOH��+NH4��
C���ö��Ե缫��ⱥ���Ȼ�����Һ��2Cl��+2H�� H2��+Cl2��
H2��+Cl2��
D��Na2SO3��Һʹ����KMnO4��Һ��ɫ��5SO32��+6H��+2MnO4�� 5SO42��+2Mn2��+3H2O
5SO42��+2Mn2��+3H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017����������и������µڶ����ܿ����ۻ�ѧ�������棩 ���ͣ������
(14��)�����ڹ�ũҵ�����������ȶ�������Ҫ���塣
��1����ҵ����CO2��NH3Ϊԭ����һ�������ºϳ����صĻ�ѧ����ʽΪCO2(g)+2NH3(g)  CO(NH2)2|(s)+H2O(g)�����¶����ߣ����صIJ��ʽ��͡���÷�Ӧ�ġ�H____0(�>����<��)������Ӧ��ϵ���ݻ�Ϊ1L��ij�¶���ͨ��1molCO2��2molNH3��2minʱ�ﵽƽ�⣬H2O(g)�����ʵ���Ϊ0.8mol����0��2minʱ����ڷ�Ӧ����v(NH3)=______mol/(L��min)���÷�Ӧ��ƽ�ⳣ���ɱ�ʾΪK=_______��
CO(NH2)2|(s)+H2O(g)�����¶����ߣ����صIJ��ʽ��͡���÷�Ӧ�ġ�H____0(�>����<��)������Ӧ��ϵ���ݻ�Ϊ1L��ij�¶���ͨ��1molCO2��2molNH3��2minʱ�ﵽƽ�⣬H2O(g)�����ʵ���Ϊ0.8mol����0��2minʱ����ڷ�Ӧ����v(NH3)=______mol/(L��min)���÷�Ӧ��ƽ�ⳣ���ɱ�ʾΪK=_______��
��2���ϳɰ���ԭ��֮һΪ����������Ȼ��Ϊԭ���Ʊ�������ԭ�����£�
CH4(g)+H2O(g)=CO(g)+3H2(g) ��H>0
���д�ʩһ����ʹƽ����ϵ�������ٷֺ����������______
A�������¶� B������ˮ����Ũ�� C��������� D����Сѹǿ
��3��T��ʱ����1molCO��H2�Ļ��������0.2molH2O(g)��ϣ�������ӦCO(g)+H2O(g) CO2(g)+H2(g) ��H<0���õ�1.18molCO��CO2��H2�Ļ�����壬���CO��ת����Ϊ90%,��ԭ���������CO��H2�������Ϊ_______�����������ݻ�Ϊ2L�����¶���ƽ�ⳣ��K=_______��
CO2(g)+H2(g) ��H<0���õ�1.18molCO��CO2��H2�Ļ�����壬���CO��ת����Ϊ90%,��ԭ���������CO��H2�������Ϊ_______�����������ݻ�Ϊ2L�����¶���ƽ�ⳣ��K=_______��
��4���ں����ܱ������з�����ӦCO(g)+H2O(g) CO2(g)+H2(g) ��H<0����֪c(H2)�淴Ӧʱ��t�ı仯��ͼ��������I��ʾ������ʼʱ�������ݻ��������ܱ�������1/2,�����������䣬����ͼ���л���c(H2)�淴Ӧʱ��t�ı仯����II��
CO2(g)+H2(g) ��H<0����֪c(H2)�淴Ӧʱ��t�ı仯��ͼ��������I��ʾ������ʼʱ�������ݻ��������ܱ�������1/2,�����������䣬����ͼ���л���c(H2)�淴Ӧʱ��t�ı仯����II��

��5��ͼ������һ���¶Ⱥ�ѹǿ�ºϳɰ���Ӧ��H2��N2����ʼ���ʵ���֮����NH3ƽ����������Ĺ�ϵ��ͼ��a��ĺ�����Ϊ______����������վ����֮��Ͷ�ϣ��ﵽƽ��ʱN2���������Ϊ14.5%,��a���������Ϊ______��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com