
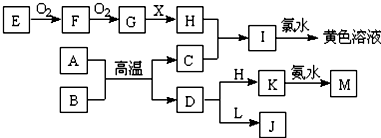
���� A��C��Ϊ�����Ľ������ʣ�A��C�����H��Ũ��Һ�о��ᷢ���ۻ�����A��CΪFe��Al��H����ΪŨ�����Ũ���ᣬA��B֮��ķ�ӦΪ���ȷ�Ӧ������BΪ��ɫ���������ӦΪFe2O3����AΪAl��CΪFe��DΪA12O3��EΪ����ǽ������ʣ�ӦΪS����FΪSO2��GΪSO3��HΪH2SO4��XΪ������ɫҺ�壬ӦΪH2O��IΪFeSO4��L��ɫΪ��ɫ������ʹ��̪��죬������Al2O3��Ӧ����LΪNaOH����Al2O3��Ӧ����J��JΪNaAlO2��A12O3�����ᷴӦ����Al2��SO4��3����KΪAl2��SO4��3��MΪAl��OH��3���������ʵ������Լ�ת����ϵ�����⣮
��� �⣺A��C��Ϊ�����Ľ������ʣ�A��C�����H��Ũ��Һ�о��ᷢ���ۻ�����A��CΪFe��Al��H����ΪŨ�����Ũ���ᣬA��B֮��ķ�ӦΪ���ȷ�Ӧ������BΪ��ɫ���������ӦΪFe2O3����AΪAl��CΪFe��DΪA12O3��EΪ����ǽ������ʣ�ӦΪS����FΪSO2��GΪSO3��HΪH2SO4��XΪ������ɫҺ�壬ӦΪH2O��IΪFeSO4��L��ɫΪ��ɫ������ʹ��̪��죬������Al2O3��Ӧ����LΪNaOH����Al2O3��Ӧ����J��JΪNaAlO2��A12O3�����ᷴӦ����Al2��SO4��3����KΪAl2��SO4��3��MΪAl��OH��3��
��1����̼����0.04%��2.3%֮�����Ͻ�Ϊ�֣�
�ʴ�Ϊ��D��
��2����������ķ�����֪��FΪSO2��
�ʴ�Ϊ��SO2��
��3��KΪAl2��SO4��3��K�백ˮ��Ӧ�����ӷ���ʽΪAl3++3 OH-=Al ��OH��3����
�ʴ�Ϊ��Al3++3 OH-=Al ��OH��3����
��4��A��B֮��ķ�ӦΪ���ȷ�Ӧ������BΪ��ɫ���������ӦΪFe2O3����AΪAl��CΪFe��DΪA12O3����Ӧ�Ļ�ѧ����ʽΪFe2O3+2Al $\frac{\underline{\;����\;}}{\;}$A12O3+2Fe��
�ʴ�Ϊ��Fe2O3+2Al $\frac{\underline{\;����\;}}{\;}$A12O3+2Fe��
��5��D��L�ķ�ӦΪAl2O3��NaOH�ķ�Ӧ������NaAlO2��ˮ����Ӧ�Ļ�ѧ����ʽΪAl2O3+2OH-=2AlO2-+H2O��
�ʴ�Ϊ��Al2O3+2OH-=2AlO2-+H2O��
���� ���⿼��������ƶϣ���Ŀ�ѶȽϴ���ע�����Ϊ��ͼʽ�����ƶ��⣬��ɴ�����Ŀ��Ҫ������Ŀ������������ץס����ͻ�ƿڣ�ֱ�ӵó����ۣ�Ȼ����˳���������������м��ƶϣ���һ�����������ۣ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ̼��̼�Ļ������������������е�Ӧ�÷dz��㷺�����ᳫ���������ѳɳ����Ľ��죬����̼�������ֻ��һ�����룬����һ��ֵ���ڴ����µ����ʽ��
̼��̼�Ļ������������������е�Ӧ�÷dz��㷺�����ᳫ���������ѳɳ����Ľ��죬����̼�������ֻ��һ�����룬����һ��ֵ���ڴ����µ����ʽ��| ʵ���� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | |
| H2O | CO | CO2 | |||
| 1 | 650 | 2 | 4 | 1.6 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 3 |
| 3 | 900 | 1 | 2 | 0.4 | 1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.1mol•L-1 H2SO4 ��Һ��ָ�������������Ϊ9.8 g | |
| B�� | ��1L0.5mol•L-1 H2SO4��Һ��ȡ��100mL����ȡ����Һ�����ʵ���Ũ��Ϊ0.5mol•L-1 | |
| C�� | ȡ0.1mol•L-1H2SO4��Һ10mL����100mLˮϡ�ͺ�H2SO4�����ʵ���Ũ��Ϊ0.01mol•L-1 | |
| D�� | 150mL 1mol•L-1��NaCl��Һ��75mL1mol•L-1��AlCl3��ҺCl-Ũ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.045mol/L | B�� | 0.036mol/L | C�� | 0.026mol/L | D�� | 0.030mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CH4 | B�� | C5H12 | C�� | C8H18 | D�� | C9H20 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
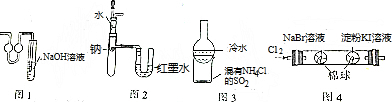
| A�� | ͼ1װ�����ڶ�������β�������� | |
| B�� | ͼ2װ��������֤Na��ˮ��Ӧ����ЧӦ | |
| C�� | ����ͼ3װ���е��ձ�������SiO2��NH4Cl | |
| D�� | ͼ4װ������֤�������ԣ�Cl2��Br2��I2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com