
| A. | Ql>Q2 | |
| B. | 反应物总能量均高于生成物总能量 | |
| C. | 1molHBr(g)具有的能量大于1molHBr(l)具有的能量 | |
| D. | 反应①生成2 molHCl(l)时放出Q1热量 |
分析 A.非金属性Cl>Br,则HCl比HBr稳定;
B.燃烧反应为放热反应;
C.同种物质气态比液体能量高;
D.由反应①可知,为生成气态HCl的能量变化.
解答 解:A.非金属性Cl>Br,则HCl比HBr稳定,则反应①中放出热量多,则Ql>Q2,故A正确;
B.燃烧反应为放热反应,则反应物总能量均高于生成物总能量,故B正确;
C.同种物质气态比液体能量高,则1molHBr(g)具有的能量大于1molHBr(l)具有的能量,故C正确;
D.由反应①可知,为生成气态HCl的能量变化,气态转化为液体时放热,则生成2 molHCl(l)时放出热量大于Q1,故D错误;
故选D.
点评 本题考查反应热与焓变,为高频考点,把握稳定性与能量的关系、反应中能量变化为解答该题的关键,侧重分析与应用能力的考查,注意物质的状态,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A | B | C | D |
| Al2O3 | Na2O2 | Si | Na2SiO3 |
| 两性氧化物 | 碱性氧化物 | 单质 | 硅酸盐 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 烧碱、纯碱、熟石灰都是碱 | B. | 铝土矿、水玻璃、小苏打都是混合物 | ||
| C. | Na2O、Al2O3、Fe2O3都是碱性氧化物 | D. | H2SO4、KOH、NaCl都是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作与现象 | 结论 |
| A | 向油脂皂化反应后的溶液中滴入酚酞,溶液变红 | 油脂已经完全皂化 |
| B | 蔗糖溶液在稀硫酸存在下水浴加热一段时间后,再与银氨溶液混合加热,有光亮的银生成 | 蔗糖溶液已经水解完全 |
| C | 向溶液X中滴入NaHCO3溶液,产生无色气体 | X中的溶质一定是酸 |
| D | 向鸡蛋清溶液中滴加醋酸铅溶液,产生白色沉淀,加水沉淀不消失 | 蛋白质发生了变性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 催化剂是影响化学反应速率的本质因素 | |
| B. | 当反应体系容积不变时,减小反应物的量肯定能降低反应速率 | |
| C. | 可逆反应达到反应限度时,化学反应速率为0 | |
| D. | 化学反应速率可用单位时间内反应物的浓度变化量来表示 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用25 mL量筒量取4.0 mol/L的盐酸5.62 mL | |
| B. | 做蒸馏操作时,冷凝水方向是下进上出 | |
| C. | 用溶解、过滤、蒸发的方法分离氯化钠与硝酸钾的混合物 | |
| D. | 用蒸发皿灼烧胆矾(CuSO4•5H2O)得到CuSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Na+、NO3-、Br- | B. | Na+、NH4+、NO3-、Cl- | ||
| C. | K+、Na+、HCO3-、NO3- | D. | K+、Cu2+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
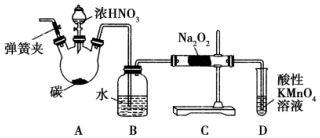 亚硝酸钠(NaNO2)被称为工业盐,在漂白、电镀等方面应用广泛.以木炭、浓硝酸、水为原料制备亚硝酸钠的装置如图所示.
亚硝酸钠(NaNO2)被称为工业盐,在漂白、电镀等方面应用广泛.以木炭、浓硝酸、水为原料制备亚硝酸钠的装置如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com