
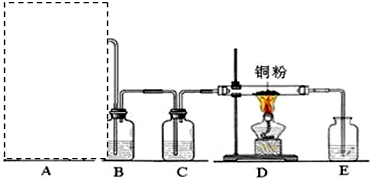
分析 (1)二氧化锰与浓盐酸在加热条件下反应生成氯气、氯化锰和水,依据反应物状态和反应条件选择发生装置;
(2)浓盐酸易挥发制备的氯气中含有氯化氢,氯化氢易溶于水,氯气在饱和食盐水中溶解度不大;
(3)制取的氯气中含有水蒸气,应进行干燥,浓硫酸具有吸水性可以干燥氯气;
(4)氯气有毒,不能直接排放到空气,应用氢氧化钠进行尾气吸收,氯气与氢氧化钠反应生成氯化钠和次氯酸钠和水.
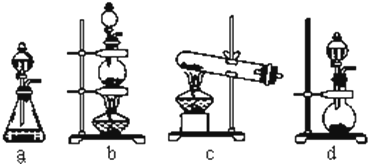
解答 解:(1)二氧化锰与浓盐酸在加热条件下反应生成氯气、氯化锰和水,方程式MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2↑+Cl2+2H2O;该反应物固体与液体,反应条件为加热,所以应选择装置b作为发生装置;
故答案为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2↑+Cl2+2H2O; b;
(2)浓盐酸易挥发制备的氯气中含有氯化氢,氯化氢易溶于水,氯气在饱和食盐水中溶解度不大,所以可以用饱和食盐水除去氯气中的氯化氢,
故答案为:吸收HCl气体;
(3)制备的氯气中含有水蒸气,浓硫酸具有吸水性,所以C处盛放的试剂浓硫酸(填名称),其作用是干燥氯气;
故答案为:浓硫酸; 干燥氯气;
(4)氯气有毒,不能直接排放到空气,应用氢氧化钠进行尾气吸收,所以E处盛有氢氧化钠溶液,氯气与氢氧化钠反应生成氯化钠和次氯酸钠和水,离子方程式:2OH-+Cl2=Cl-+ClO-+H2O;
故答案为:氢氧化钠; 2OH-+Cl2=Cl-+ClO-+H2O.
点评 本题考查了氯气的制备和净化,明确氯气制备原理及氯气的性质是解题关键,注意发生装置选择应依据反应物状态和反应条件选择.


科目:高中化学 来源: 题型:选择题
 ,其中R1、R2为烷烃基.正确的是( )
,其中R1、R2为烷烃基.正确的是( )| A. | 若R1=R2,一定条件下,则始祖鸟烯环上的一氯代物有2种 | |
| B. | 若R1=R2=CH3,则其化学式为C12H16 | |
| C. | 始祖鸟烯与乙烯互为同系物 | |
| D. | 始祖鸟烯既能使酸性高锰酸钾褪色也能使溴水褪色,且褪色原理相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Z2与X-在水溶液中不能大量共存 | |
| B. | 还原性:Y->Z->W- | |
| C. | 2NaW+Y2=2NaY+W2 | |
| D. | W2通入到NaX和NaY的混合溶液中:W2优先氧化Y- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 固体悬浮微粒是造成雾霾天气的一种重要因素 | |
| B. | 一氧化碳、氮氧化物是酸雨形成的主要因素 | |
| C. | 含铅化合物导致人体蛋白质变性是物理变化 | |
| D. | 汽车尾气可通过净化装置将碳氢化合物还原成CO2和H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
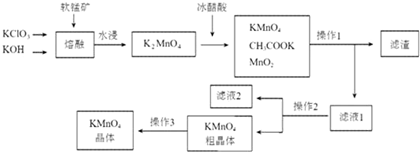
| 物质 温度 | KMnO4 | CH3COOK | K2SO4 | KCl |
| 20℃ | 6.34 | 217 | 11.1 | 34.2 |
| 90℃ | 45.2 | 398 | 22.9 | 53.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | C | N | O | F | Ne | |||
| 3 | Na | Al | P | S | Cl |
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:推断题
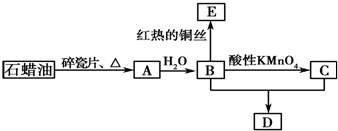
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com