
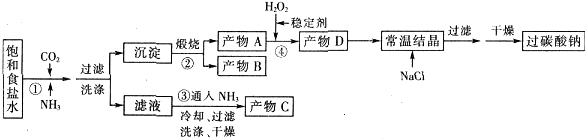
| A.FeCl3溶液 | B.H2S | C.稀硫酸 | D.NaHCO3溶液 |
| T/℃ | 活性氧百分含量 | 产率 |
| 5~10 | 13.94 | 85.49 |
| 10~15 | 14.02 | 85.78 |
| 15~20 | 15.05 | 88.38 |
| 20~25 | 14.46 | 83.01 |
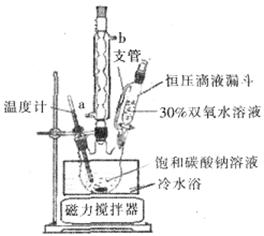 、
、

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:问答题
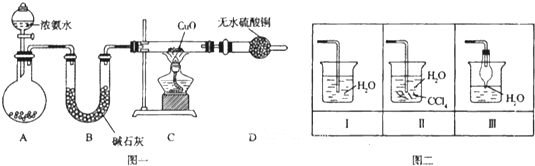
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题


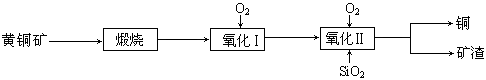
| 沸腾炉温度/℃ | 560 | 580 | 600 | 620 | 640 | 660 |
| 水溶性Cu/% | 90.12 | 91.24 | 93.50 | 92.38 | 89.96 | 84.23 |
| 酸溶性Cu/% | 92.00 | 93.60 | 97.08 | 97.82 | 98.16 | 98.19 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题


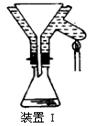
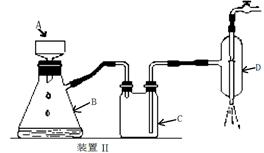

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
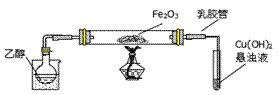
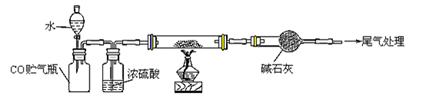
 =_____。
=_____。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 编号 | 仪器 | 药品 | 实验目的 |
| A | 托盘天平(带砝码)、250mL容量瓶、量筒、烧杯、药匙、玻玻棒 | NaOH固体、蒸馏水 | 配制250mL一定物质的量浓度的NaOH溶液 |
| B | 分液漏斗、锥形瓶、导管及橡皮塞 | 稀硫酸、碳酸钠、硅酸钠溶液 | 证明非金属性;S>C>Si |
| C | 碱式滴定管、酸式滴定管、胶头滴管、铁架台(带铁夹)、锥形瓶 | 己知浓度的NaOH溶液、待测盐酸、蒸馏水、白纸 | 测定稀盐酸的物质的量浓度 |
| D | 铁架台(带铁夹)、酒精灯、大试管、集气瓶、导管及橡皮塞 | 氯化铵 | 制取氨气 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
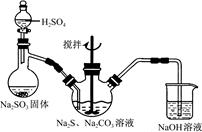
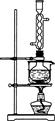
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com