
下列5种有机化合物中,能够发生酯化、加成和氧化三种反应的是
① CH2=CHCOOH ② CH2=CHCOOCH3 ③ CH2=CHCH2OH
④ CH3CH2CH2OH ⑤ 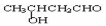
A.①③④ B.②④⑤ C.①③⑤ D.①②⑤
科目:高中化学 来源:2016届安徽省合肥市高三上学期期中考试化学试卷(解析版) 题型:选择题
利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液。则下列说法不正确的是 ( )
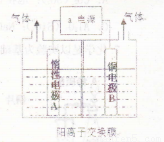
A.外加电源的a极为正极
B.电解过程中,Li+向B极迁移
C.阳极反应式为:4OH--4e-=O2↑+H2O
D.每生成1molLiOH,外电路转移1mol电子
查看答案和解析>>
科目:高中化学 来源:2015-2016学年贵州省高二上二次月考化学试卷(解析版) 题型:选择题
在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g) 2Z(g)△H<0,一段时间后达到平衡,反应过程中测定的数据如下表.下列说法正确的是
2Z(g)△H<0,一段时间后达到平衡,反应过程中测定的数据如下表.下列说法正确的是
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A.反应前2min的平均速率v(Z)=2.0×10﹣5mol/(L·min)
B.其他条件不变,降低温度,反应达到新平衡前v(逆)>v(正)
C.该温度下此反应的平衡常数K=1.44
D.其他条件不变,再充入0.2mol Z,平衡时X的体积分数增大
查看答案和解析>>
科目:高中化学 来源:2016届云南师大附属中学高三上适应性月考理综化学试卷(解析版) 题型:填空题
铁是目前人类使用量最大的金属,它能形成多种化合物.
(l)工业上,向炽热铁屑中通入氯化氢可生成无水氯化亚铁,若操作不当,制得的FeCl2会含有少量FeCl3,检验FeCl3,常用的试剂是 ;为防止FeC12溶液中含有FeCl3,最好在FeCl2溶液中加入
(2)LiFePO4(难溶于水)材料被视为最有前途的锂离子电池材料之一。
①以FePO4(难溶于水)、Li2CO3、单质碳为原料在高温下制备LiFePO4,同时伴随产生一种可燃性气体,该反应的化学方程式为 。若有1mol C参与反应,则转移的电子数目为
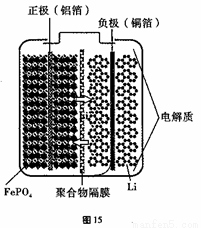
②磷酸铁锂动力电池有几种类型,其中一种(中间是锂离子聚合物的隔膜,它把正极与负极隔开,只允许锂离子通过)工作原理为FePO4+Li LiFePO4。如图所示,则放电时FePO4一端为电池的 极,充电时阳极上的电极反应式为______________________________。
LiFePO4。如图所示,则放电时FePO4一端为电池的 极,充电时阳极上的电极反应式为______________________________。
(3)硫化亚铁常用于工业废水的处理。已知25℃时,溶度积常数Ksp[FeS]=6.3×10-18,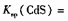 3.6×10-29。请写出用硫化亚铁处理含Cd2十的工业废水的离子方程式:
3.6×10-29。请写出用硫化亚铁处理含Cd2十的工业废水的离子方程式:
在FeS、CdS的悬浊液中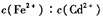 =
=
(4)已知25℃时,尺,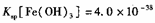 ,此温度下若在实验室中配制
,此温度下若在实验室中配制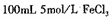 溶液,为使配制过程中不出现浑蚀现象,则至少需要加入 mL 2lnol/L的盐酸〔体积变化忽略不计)
溶液,为使配制过程中不出现浑蚀现象,则至少需要加入 mL 2lnol/L的盐酸〔体积变化忽略不计)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上期中测试化学试卷(解析版) 题型:选择题
(改编)某学习兴趣小组讨论辨析以下说法,其中说法正确的是
①通过化学变化可以实现16O与18O间的相互转化②灼烧钠的化合物时,火焰呈黄色,发生化学反应
③碱性氧化物一定是金属氧化物④只由一种元素组成的物质一定为纯净物
⑤石墨和C60是同素异形体⑥糖类、蛋白质、油脂属于天然高分子化合物
A.③⑤⑥ B.①② C.③⑤ D.①③④
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁实验中学分校高二上12月月考化学卷(解析版) 题型:填空题
根据题干要求回答下列问题
(1)用系统命名法给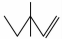 命名为:_________________;写出该物质与HBr反应的化学方程式:_________________
命名为:_________________;写出该物质与HBr反应的化学方程式:_________________
(2)2?丁烯合成聚2?丁烯的方程式为:_________________________
(3)实验室制乙烯的反应方程式:______________________________
2-甲基-1,2-丁二醇的催化氧化方程式: __________________________
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二上12月月考化学试卷(解析版) 题型:填空题
煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程。
(1)将水蒸气通过红热的碳即可产生水煤气。反应为:
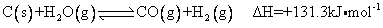
一定温度下,在一个容积固定的密闭容器中,发生上述反应,下列不能判断该反应达到化学平衡状态的是___________________(填字母)。
a.容器中的压强不变
b.1 mol H-H键断裂的同时断裂2 mol H-O键
c. 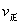 (CO)=
(CO)=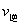 (H2O)
(H2O)
d.c (CO) = c (H2)
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2 L的恒容密闭容器中,进行反应
CO(g)+H2O(g) ? CO2 (g)+H2 (g) ,得到如下三组数据:
实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
H2O | CO | H2 | CO2 | |||
1 | 650 | 2 | 4 | 1.6 | 1.6 | 5 |
2 | 900 | 1 | 2 | 0.4 | 0.4 | 3 |
3 | 900 | a | b | c | d | t |
①该反应的逆反应为____________(填“吸”或“放”)热反应
②若实验3要达到与实验2中各物质的质量分数分别相等,且t<3min,则a、b应满足的关系是______________(用含a、b的数学式表示)。
(3)目前工业上有一种方法是用CO2来生产甲醇。一定条件下发生反应:
CO2 (g)+3H2 (g)  CH3OH(g)+H2O(g)右图表示该反应进行过程中能量(单位为kJ?mol。)的变化。
CH3OH(g)+H2O(g)右图表示该反应进行过程中能量(单位为kJ?mol。)的变化。
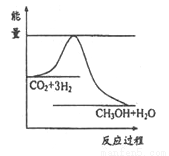
①在体积为1 L的恒容密闭容器中,充入l molCO2和3molH2,下列措施中能使 c (CH3OH)增大的是_______(填字母)
a.升高温度
b.充入He (g),使体系压强增大
c.将H2O(g)从体系中分离出来
d.再充入l mol CO2和3 molH2
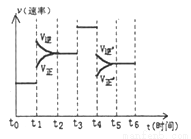
②当反应达到平衡时不断改变条件(但不改变各组分物质的量和状态)反应速率随时间的变化如右图:其中表示平衡混合物中CH3OH含量最高的一段时间是_______________;如t0~t1平衡常数为K1, t2~t3平衡常数为K2 ,则K1_______________K2(填“大于”、“等于”或“小于”)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高二上学期期中选修化学试卷(解析版) 题型:填空题
80℃时,将0.40mol的N2O4气体充入2L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4  2NO2 △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
2NO2 △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
时间(s) n(mol) | 0 | 20 | 40 | 60 | 80 | 110 |
n(N2O4) | 0.40 | a | 0.20 | c | d | e |
n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
①计算20s—40s内用N2O4表示的平均反应速率为 mol/(L.s)
②计算在80℃时该反应的N2O4的转化率= 此温度下
③反应进行至110s后将反应混合物的温度降低,混合气体的颜色 ;如果此时加入NO2,则此时容器内颜色 (填“变浅”、“变深”或“不变”)
④要增大该反应NO2 的体积分数,可采取的措施有(填序号)
A.增大N2O4的起始浓度 B.通入N2气体
C.使用高效催化剂 D.升高温度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com