
| A、蛋白质、纤维素、蔗糖、天然橡胶、淀粉都是高分子化合物 |
| B、乙烯和苯都能使溴水褪色,褪色的原因相同 |
| C、淀粉、葡萄糖、脂肪和蛋白质在一定条件下都能发生水解反应 |
| D、米酒变酸的过程涉及了氧化反应 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、反应后溶液中离子浓度大小关系为:c(K+)>c(NO3-)>c(Ag+)>c(Cl-)>c(I-) |
| B、发生反应生成的AgI沉淀多于AgCl沉淀 |
| C、在水中AgCl的溶解度比AgI的溶解度大 |
| D、若在AgCl悬浊液中滴加KI溶液,白色沉淀会转变成黄色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 有关物质存在如图所示的转化关系(部分产物已省略).通常C为气体单质,G为紫黑色固体单质.实验室中,常用固体E在B的催化下加热制取气体单质H.
有关物质存在如图所示的转化关系(部分产物已省略).通常C为气体单质,G为紫黑色固体单质.实验室中,常用固体E在B的催化下加热制取气体单质H.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、聚乙烯食品包装袋、食物保鲜膜都是无毒的高分子化合物 |
| B、“地沟油”危害健康,主要是人体所必需的维生素E、脂肪酸油脂已经被破坏 |
| C、太阳能电池板中的硅是硅单质,光导纤维的主要成分是二氧化硅,红宝石、珍珠、玛瑙、水晶、钻石等装饰品的主要成分都是硅酸盐 |
| D、石油裂解、煤的气化、海水制镁等过程中都包含化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
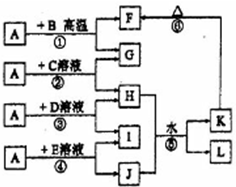 如图所示,A、G、I均为单质,其中A、G为金属且都常被用作输电导线材料,B为黑色粉末,L是由两种元素组成的盐,它是家庭厨房必备物品.请回答:
如图所示,A、G、I均为单质,其中A、G为金属且都常被用作输电导线材料,B为黑色粉末,L是由两种元素组成的盐,它是家庭厨房必备物品.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、Mg2+、Cl-、SO42- |
| B、K+、NH4+、OH-、NO3- |
| C、Na+、Ca2+、CO32-、Cl- |
| D、Na+、H+、CO32-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、16gO2中含有的氧气分子数为0.5NA |
| B、常温常压下,1molNe含有的原子数为NA |
| C、1.6gCH4中含有的甲烷分子数为0.1NA |
| D、1mol/LNaCl溶液中含有的钠离子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| Fe2O3 | CO | Fe | CO2 | |
| 甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| 乙/mol | 1.0 | 1.5 | 1.0 | 1.0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com