
【题目】下列情况,离子可能大量共存的是( )
A.Al3+、Na+、Cl-、CO32-
B.25℃,水电离出的OH-浓度为10-11mol/L的溶液中:K+、Na+、SO32-、NO3-
C.![]() =10-2溶液中:Cu2+、Na+、Cl-、NO3-
=10-2溶液中:Cu2+、Na+、Cl-、NO3-
D.无色溶液中:H+、Fe2+、Cl-、NH4+
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】常温下,用NaOH溶液作![]() 捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品
捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品![]()
(1)若某次捕捉后得到![]() 的溶液,则溶液中
的溶液,则溶液中![]() :
:![]() ______
______![]() 常温下
常温下![]() 、
、![]() ,
,
(2)欲用5L![]() 溶液将
溶液将![]()
![]() 固体全都转化为
固体全都转化为![]() ,则所用的
,则所用的![]() 溶液的物质的量浓度至少为______。
溶液的物质的量浓度至少为______。![]() 已知:常温下
已知:常温下![]() 、
、![]() 忽略溶液体积的变化
忽略溶液体积的变化![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合金是建造航空母舰的主体材料.
(1)航母升降机可由铝合金制造.
①铝元素在周期表中的位置为 ______ ![]() 工业用铝土矿冶炼铝的化学方程式 ______ .
工业用铝土矿冶炼铝的化学方程式 ______ .
②![]() 合金焊接前用NaOH溶液处理
合金焊接前用NaOH溶液处理![]() 膜,其化学方程式为 ______ .
膜,其化学方程式为 ______ .
(2)![]() 也是重要的铝盐,其无水
也是重要的铝盐,其无水![]() 升华
升华![]() 遇潮湿空气即产生大量白雾,实验室可用下列装置制备.
遇潮湿空气即产生大量白雾,实验室可用下列装置制备.
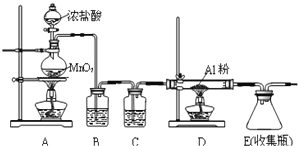
①装置在实验开始前应 ______ ,操作方法是: ______ .
②装置B中盛放饱和NaCl溶液,该装置的主要作用是 ______ ![]() 装置C中盛放 ______ .
装置C中盛放 ______ .
③装置A中发生的离子反应 ______ .
④该装置缺少尾气处理装置,尾气处理装置用的仪器是 ______ 装碱石灰.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】425℃时,在两个1L密闭容器中分别发生化学反应,物质的浓度随时间的变化如图所示。下列叙述错误的是( )
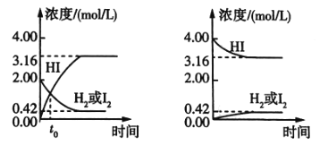
A.图①中t0时,三种物质的物质的量相等
B.图①中![]() 时,反应达到平衡状态
时,反应达到平衡状态
C.图②中的可逆反应为2HI(g)![]() H2(g)+I2(g)
H2(g)+I2(g)
D.图①②中,当c(HI)=3.16mol/L时,两容器中的反应均达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某纯碱试样中含有NaCl杂质,有多种方法测定试样中纯碱的质量分数。
![]() 气体法
气体法
可用图中的装置进行实验:

主要实验步骤如下:
![]() 按图组装仪器,并检查装置的气密性;
按图组装仪器,并检查装置的气密性;
![]() 将ag试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液;
将ag试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液;
![]() 从A处导管缓缓鼓入一定量的空气;
从A处导管缓缓鼓入一定量的空气;
![]() 称量盛有碱石灰的U型管的质量,得到b克;
称量盛有碱石灰的U型管的质量,得到b克;
![]() 从分液漏斗滴入
从分液漏斗滴入![]() 的盐酸,直到不再产生气体时为止;
的盐酸,直到不再产生气体时为止;
![]() 再从A处导管缓缓鼓入一定量的空气;
再从A处导管缓缓鼓入一定量的空气;
![]() 再次称量盛有碱石灰的U型管的质量,得到c克;
再次称量盛有碱石灰的U型管的质量,得到c克;
![]() 重复步骤
重复步骤![]() 和
和![]() 的操作,直到U型管的质量基本不变,为d克;
的操作,直到U型管的质量基本不变,为d克;
请填空和回答问题:
![]() 、D两装置中分别装什么试剂C: ______ D: ______
、D两装置中分别装什么试剂C: ______ D: ______
![]() 装置中干燥管F的作用是 ______
装置中干燥管F的作用是 ______
![]() 该试样中纯碱的质量分数的计算式为 ______
该试样中纯碱的质量分数的计算式为 ______
![]() 沉淀法
沉淀法
称取![]() 克样品完全溶于水后加足量的
克样品完全溶于水后加足量的![]() 溶液,然后过滤、洗涤、干燥称重得
溶液,然后过滤、洗涤、干燥称重得![]() 克固体,在该实验洗涤操作中如何检验固体已洗干净 ______ 。
克固体,在该实验洗涤操作中如何检验固体已洗干净 ______ 。
![]() 滴定法
滴定法
准确称取![]() 克样品,溶于水配成250mL溶液,量取25.00mL溶液于锥形瓶中,加入几滴酚酞作指示剂,用
克样品,溶于水配成250mL溶液,量取25.00mL溶液于锥形瓶中,加入几滴酚酞作指示剂,用![]() 的盐酸溶液进行滴定,到达终点时共消耗20.00mL盐酸,则样品中纯碱的质量分数为 ______ ,以下实验操作导致测量结果偏低的是 ______
的盐酸溶液进行滴定,到达终点时共消耗20.00mL盐酸,则样品中纯碱的质量分数为 ______ ,以下实验操作导致测量结果偏低的是 ______
A.配制样品溶液定容时俯视容量瓶刻度线
B.配制样品溶液定容后摇匀,发现液面低于容量瓶刻度线,于是又加水至刻度线
C.用盐酸滴定时滴定前仰视刻度线读数,滴定终点时俯视刻度线读数
D.滴定前锥形瓶中有水
E.酸式滴定管滴定前有气泡,而滴定后气泡消失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设![]() 为阿伏加德罗常数的值,下列叙述正确的是( )
为阿伏加德罗常数的值,下列叙述正确的是( )
A.标准状况下,![]() 分子中含有
分子中含有![]()
![]() 个碳氧双键
个碳氧双键
B.一定温度下,![]() 完全反应转移的电子数一定为
完全反应转移的电子数一定为![]()
![]()
C.常温常压下,![]() 固体中离子总数为
固体中离子总数为![]()
![]()
D.常温常压下,![]() 溶液中
溶液中![]() 和
和![]() 数目之和为
数目之和为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,容积为2L的密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图所示。
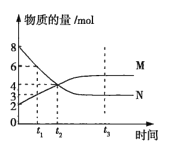
(1)该反应的化学方程式为___。
(2)比较t2、t3时正、逆反应速率的大小(用v正、v逆表示):t2时__;t3时__。
(3)若t2=2min,则反应开始至t2时,M的平均反应速率为__。
(4)下列说法可以表明该反应已达到平衡状态的是__(填序号)。
A.混合气体的密度不变
B.正、逆反应速率都等于零
C.M、N的物质的量浓度不变
D.M、N的物质的量浓度相等
(5)t3时化学反应达到平衡状态,请写出3个可以提高此时该反应化学反应速率的方法:__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,等容积的两容器内分别充满![]() 和
和![]() 气体。下列说法正确的是
气体。下列说法正确的是
A.所含分子数和质量均不相同
B.含有相同的分子数和电子数
C.含有相同的质子数和中子数
D.含有相同数目的中子、原子和分子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com