


科目:高中化学 来源:不详 题型:单选题
| A.RO2 | B.RO3 | C.R2O3 | D.R2O5 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.4.6克钠与水反应时失去的电子数目为0.2NA |
| B.常温常压下2克氢气所含原子数目为NA |
| C.在标准状况下,22.4LNH3所含的分子数目为NA |
| D.1 L0.5mol?L-1Na2SO4溶液中所含有的Na+离子数目为NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.常温常压下,22.4 L CH4中含有的C—H键数为4NA |
| B.4.6 g由NO2和N2O4组成的混合气体中含有的氧原子数为0.3NA |
| C.含0. 2 mol H2SO4的浓硫酸与足量Cu反应,生成SO2的分子数为0.1NA |
| D.1 mol Na在足量O2中燃烧生成Na2O2,钠失去的电子数为NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| A.烧杯中溶液转移到容量瓶中时,未洗涤烧杯 |
| B.定容时,俯视刻度线 |
| C.定容时,仰视刻度线 |
| D.移液时,有少量液体溅出 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.溶液中c(Na+)=2c(SO42-) |
B. mol>沉淀的物质的量>0 mol>沉淀的物质的量>0 |
C.沉淀的物质的量= mol mol |
D.原浓硫酸中H2SO4的物质的量> mol mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.所得溶液的物质的量浓度为1 mol/L |
| B.所得溶液中含有NA个HCl分子 |
| C.36.5 g HCl气体占有的体积为22.4 L |
| D.所得溶液的质量分数:w="36.5c/(1" 000ρ) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.图中A点溶液的pH=1 |
| B.生成沉淀的最大质量为2.33g |
| C.原混合溶液中盐酸物质的量浓度为0.1mol/L |
D.当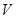 [Ba(OH)2(aq)]=10mL时,发生反应的离子方程式为:Ba2++SO [Ba(OH)2(aq)]=10mL时,发生反应的离子方程式为:Ba2++SO ═BaSO4↓ ═BaSO4↓ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com