
【题目】下列变化过程一定属于还原反应的是( )
A. HCl→MgCl2 B. Na→Na+
C. CO→CO2 D. Fe3+→Fe2+
科目:高中化学 来源: 题型:
【题目】氮化硅(Si3N4)是一种优良的高温结构陶瓷,在工业生产和科技领域中有重要用途。
Ⅰ.工业上有多种方法来制备氮化硅,下面是几种常见的方法:
(1)方法一 直接氮化法:在1300~1400 ℃时,高纯粉状硅与纯氮气化合,其反应方程式为3Si+2N2![]() Si3N4
Si3N4
(2)方法二 可以用NH3和SiH4(硅烷)在一定条件下反应,并在600 T的加热基板上生成氮化硅膜,其反应方程式为___________________。
(3)方法三 化学气相沉积法:在高温条件下利用四氯化硅气体、纯氮气、氢气反应生成氮化硅和HCl,与方法一相比,用此法制得的氮化硅纯度较高,其原因是___________________。
(4)方法四 Si(NH2)4热分解法:先用四氯化硅与氨气反应生成Si(NH2)4和一种气体__________________(填分子式);然后使Si(NH2)4受热分解,分解后的另一种产物的分子式为_________________。
Ⅱ.工业上制取高纯硅和四氯化硅的生产流程如下:
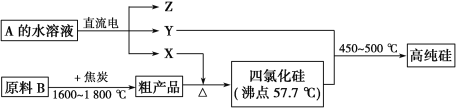
已知:X、高纯硅、原料B的主要成分都可与Z反应,Y与X在光照或点燃条件下可反应,Z的焰色呈黄色。
(1)写出焦炭与原料B中的主要成分反应的化学方程式:__________________
(2)上述生产流程中电解A的水溶液时,以Cu为阳极电解A的水溶液电解反应方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是
A. 氨气溶于醋酸溶液:NH3+H+→NH4+
B. 将硫化氢气体通入足量氢氧化钠溶液中,H2S+2OH-→S2-+2H2O
C. 向氯化亚铁溶液中加入溴水:Fe2++Br2→Fe3++2Br-
D. 碳酸氢钠溶液中加入足量的石灰水:2HCO3-+Ca2++2OH-→CaCO3↓+CO32-+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:
3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH
3Zn(OH)2+2Fe(OH)3+4KOH
下列叙述不正确的是
A.放电时负极反应为:Zn-2e-+2OH-=Zn(OH)2
B.放电时阳极反应为: Fe(OH)3+5OH--3e-= FeO42-+4H2O
C.放电时每转移3 mol电子,正极有1 mol K2FeO4被氧化
D.放电时的正极在充电时应接电源正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原电池反应的离子方程式为:Zn+2H+=Zn2++H2↑,则下列说法正确的是
A. HNO3可作电解质溶液 B. 电子从正极沿导线流向负极
C. 锌极质量不变 D. 石墨可作原电池的正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】构成DNA、唾液淀粉酶、固醇、纤维素的化学成分中,共有的化学元素是
A. C、H、0、N、P B. C、H、0、N、S
C. C、H、0 D. C、H、0、N
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】与纯水的电离相似,液氨中也存在着微弱的电离:2NH3![]() NH4++NH2-.据此判断,以下叙述错误的是
NH4++NH2-.据此判断,以下叙述错误的是
A.液氨中含有NH3、NH4+、NH2-等粒子
B.一定温度下液氨中c(NH4+)·c(NH2-)是一个常数
C.液氨达到电离平衡时c(NH3)=c(NH4+)=c(NH2-)
D.只要不加入其他物质,液氨中c(NH4+)=c(NH2-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中属于氧化还原反应,但水既不作氧化剂又不作还原剂的是( )
A.SO3+H2O===H2SO4
B.2Na2O2+2H2O===4NaOH+O2↑
C.2F2+2H2O===4HF+O2
D.2Na+2H2O===2NaOH+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温恒容条件下,下列叙述中不是可逆反应2A(g)+3B(s)![]() 2C(g)达到平衡的标志的是( )
2C(g)达到平衡的标志的是( )
①C的生成速率与C的分解速率相等
②单位时间生成amol A,同时消耗1.5amol B;
③各组分的浓度不再变化;
④混合气体的密度不再变化;
⑤混合气体的总压强不再变化;
⑥混合气体的物质的量不再变化;
⑦混合气体的平均摩尔质量不再变化;
⑧A、B、C的分子数目比为2:3:2.
A.⑤⑥⑧ B.②⑤⑧ C.①③④ D.②④⑦
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com