
| ��0.1mol/L�ı������0.01mol•L-1�ı����� | �� | ��0.1mol•L-1�ı�����ζ�δ֪Ba��OH��2��Һ10mL��ȥ����19.60mL | �� | ��Ba��OH��2��Һ����10L�����е�CO2����״���� | �� | �� �� | �� | ȡ��Һ20mL����0.01mol•L-1������ζ���ȥ����34.8mL |
���� ��1�����ñ�������Һ����Ҫ�õ��������У�����ƿ���ζ��ܡ���Ͳ���ձ�����ͷ�ιܡ���������
��2���ζ�����ʱ����������ʽ�ζ��ܻ������۾�ע����ƿ����Һ��ɫ�ı仯��
��3��Ba��OH��2��Һ�������������Ba��OH��2������е�������Ӧ������BaCO3����������˵�ԭ���dz�ȥBaCO3������ʹ��Һֻ��Ba��OH��2���Ա�֤ʵ��ɹ���
��4���ٵζ�������ζ��ܼ��촦��һ���ݣ�˵����ȡ���ı���Һ�����С��
����ʵ���У�����һ�εζ�ʱʹ�õ���ʽ�ζ���δ����������������Һ������ʽ�ζ����ڱ�մ��������Ũ�����ᣬ���еڶ��εζ�ʱ�����������������٣�����ʵ����CO2���������ֵƫ�ͣ�
�ʴ�Ϊ��ƫ�ߣ�
��5����������ͼ����������кͷ�Ӧ�����δ֪Ba��OH��2��Һ��Ũ��Ϊ $\frac{0.1mol/L��19.60ml}{2��10ml}$=9.8��10-2 mol/L���������CO2�����Ϊ��
V��CO2��=��9.8��10-2mol/L��0.01L-0.01mol/L��0.0348L��$\frac{1}{2}$��5����22.4L•mol-1=0.0025L������õ�CO2�����������
��� �⣺��1�����ñ�������Һ����Ҫ�õ��������У�����ƿ���ζ��ܡ���Ͳ���ձ�����ͷ�ιܡ�����������ѡB
�ʴ�Ϊ��B��
��2���ζ�����ʱ����������ʽ�ζ��ܻ������۾�ע��Һ���µ��ٶȺ���ƿ����Һ��ɫ�ı仯��
�ʴ�Ϊ��������ʽ�ζ��ܻ�����Һ���µ��ٶȺ���ƿ����Һ��ɫ�ı仯��
��3��Ba��OH��2��Һ�������������Ӧ������BaCO3����������˵�ԭ���dz�ȥBaCO3������ʹ��Һֻ��Ba��OH��2���Ա�֤ʵ��ɹ���
�ʴ�Ϊ����ȥBaCO3������ʹ��Һֻ��Ba��OH��2���Ա�֤ʵ��ɹ���
��4���ٱ�ʵ���У���0.1mol•L-1�ı�����ζ�δ֪Ba��OH��2��Һʱ�����ڲ����������ζ�������ζ��ܼ��촦��һ���ݣ�˵����ȡ���ı���Һ�����С��ʵ����ȥ�������19.60mL��
�ʴ�Ϊ�����ڣ�
����ʵ���У�����һ�εζ�ʱʹ�õ���ʽ�ζ���δ����������������Һ������ʽ�ζ����ڱ�մ��������Ũ�����ᣬ���еڶ��εζ�ʱ�����������������٣�����ʵ����CO2���������ֵƫ�ͣ��ʴ�Ϊ��ƫ�ͣ�
��5����������ͼ����������кͷ�Ӧ�����δ֪Ba��OH��2��Һ��Ũ��Ϊ $\frac{0.1mol/L��19.60ml}{2��10ml}$=9.8��10-2 mol/L���������CO2�����Ϊ��V��CO2��=��9.8��10-2mol/L��0.01L-0.01mol/L��0.0348L��$\frac{1}{2}$��5����22.4L•mol-1=0.0025L����CO2���������Ϊ$\frac{0.0025L}{10L}$��100%=0.025%��
�ʴ�Ϊ��0.025%��
���� ������Ҫ�����˿�����CO2�����IJⶨ���漰�ζ�ʵ��IJ��������㡢�������ȣ�ע��ʵ���ԭ������ʵ���ǽ��ʵ����Ĺؼ�����Ŀ�Ѷ��еȣ�


 ����ѧ���ʱѧ����ϵ�д�
����ѧ���ʱѧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ȼ�����ӵĵ���ʽ��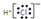 | B�� | S2-�Ľṹʾ��ͼ�� | ||
| C�� | ���Ȼ�̼�ĵ���ʽ��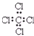 | D�� | N2���ӵĽṹʽ��N=N |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���Ʋ;߲������������Ի���Ե�ʳ�� | |
| B�� | ̼���ƿ������кͷ��������е��������� | |
| C�� | �������ƿ����ں����������������Դ | |
| D�� | ������ϩ������Ʒ������ʳƷ�İ�װ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
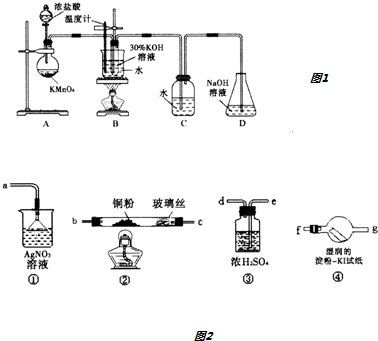
| �Թܱ�� | 1 | 2 | 3 | 4 |
| 0.20mol•L-1KI/mL | 1.0 | 1.0 | 1.0 | 1.0 |
| KClO3��s��/g | 0.10 | 0.10 | 0.10 | 0.10 |
| 6.0mol•L-1H2SO4/ml | 0 | 3.0 | 6.0 | 9.0 |
| ����ˮ/mL | 9.0 | 6.0 | 3.0 | 0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �� | B�� | �� | C�� | ��ԭ�� | D�� | ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | FeO | B�� | Fe2O3 | C�� | Fe3O4 | D�� | FeO��Fe2O3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �÷�Ӧ��Fe2+�ǻ�ԭ����O2�ǻ�ԭ���� | |
| B�� | 4 mol Na2O2�ڷ�Ӧ�й��õ�8NA������ | |
| C�� | ÿ����0.2 mol O2����Fe2+��ԭ��������Ϊ0.4 mol | |
| D�� | ��Ӧ�����п��Կ�����ɫ����ת��Ϊ����ɫ��ת��Ϊ���ɫ���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com