
某碱性溶液中,可以大量共存的离子组是
A. K+、Na+、HCO3-、NO3- B. H+、Mg2+、SO42-、NO3-
C. Na+ 、SO42-、Cl-、ClO- D.Ag+、K+、NO3-、Na+
 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源: 题型:阅读理解
 测定样品中成分含量的实验一般应重复二至三次.为了测定某NaOH固体中混有的Na2CO3的质量分数,某同学分别设计了三种实验方案:
测定样品中成分含量的实验一般应重复二至三次.为了测定某NaOH固体中混有的Na2CO3的质量分数,某同学分别设计了三种实验方案:| 106n |
| 197m |
| 106n |
| 197m |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 序号 | a | b | c | d | e | f |
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5Na |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
| c(CH3OCH3)?c(H2O) |
| c2(CH3OH) |
| c(CH3OCH3)?c(H2O) |
| c2(CH3OH) |
| 物质 | CH3OH | CHO3CH3 | H2O |
| 浓度/mol/L | 0.8 | 1.24 | 1.24 |
查看答案和解析>>
科目:高中化学 来源: 题型:
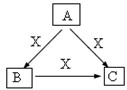 A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图.请针对以下三种不同情况回答:
A、B、C、X是中学化学常见物质,均由短周期元素组成,转化关系如图.请针对以下三种不同情况回答:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③⑥ | B、②④⑤ | C、①③④ | D、③⑤⑥ |
查看答案和解析>>
科目:高中化学 来源:湖南省月考题 题型:填空题
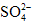 ; ②Na+、Mg2+、Cl-、
; ②Na+、Mg2+、Cl-、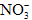 ; ③K+、Ba2+、Cl-、
; ③K+、Ba2+、Cl-、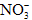 ;
; 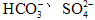
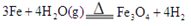

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com