
【题目】N2O5是一种新型硝化剂,其性质和制备受到人们的关注。
(1)一定温度下,在恒容密闭容器中N2O5可发生下列反应:N2O5(g)![]() 4NO2(g)+O2(g);△H>0
4NO2(g)+O2(g);△H>0
①如表为反应在T1 温度下的部分实验数据:
t/s | 0 | 500 | 1000 |
c(N2O5)/mol·L-1 | 5.00 | 3.52 | 2.48 |
则500s内N2O5的分解速率为____________________。
②在T 2温度下,反应1000s时测得NO2的浓度为4.98 mol·L-1,则T2________T1( 填>、<或=)。
(2)现以H2、O2、熔融Na2CO3组成的燃料电池采用电解法制备N2O5,装置如图所示,其中Y为CO2。
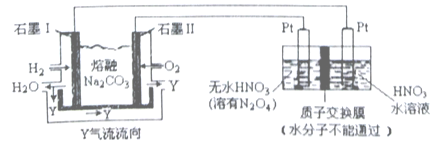
写出石墨Ⅰ电极上发生反应的电极反应式_____________________。N2O5 在电解池的_____________区生成(填“阳极”或“阴极”)。
【答案】 0.00296mol·L-1·s-1 < H2+CO32--2e-=H2O+CO2 阳极
【解析】(1). ①. 由表中数据可知,500s内N2O5的浓度变化量为△c(N2O5)=5mol/L3.52mol/L=1.48mol/L,故N2O5的分解速率为![]() =0.00296mol·L-1·s-1,故答案为:0.00296mol·L-1·s-1;
=0.00296mol·L-1·s-1,故答案为:0.00296mol·L-1·s-1;
②.在T2温度下,反应1000s时测得NO2的浓度为4.98molL1,则此时N2O5的浓度为5mol/L![]() ×4.98molL1=2.51mol/L,因该反应是吸热反应,高于在T1温度下1000s时N2O5的浓度2.48 mol/L,说明T2温度下反应逆向进行,故温度T2<T1,故答案为:<;
×4.98molL1=2.51mol/L,因该反应是吸热反应,高于在T1温度下1000s时N2O5的浓度2.48 mol/L,说明T2温度下反应逆向进行,故温度T2<T1,故答案为:<;
(2).原电池负极发生氧化反应,由装置图可知,负极上氢气失去电子,与熔融盐中碳酸根离子结合生成二氧化碳与水,负极电极反应式为:H2+CO322e═H2O+CO2,从电解原理来看,N2O4制备N2O5为氧化反应,则N2O5应在阳极区生成,故答案为:H2+CO322e═H2O+CO2;阳极。


 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:高中化学 来源: 题型:
【题目】(Ⅰ)磷是生物体中不可缺少的元素之一,在自然界中磷总是以磷酸盐的形式出现的,例如磷酸钙矿Ca3(PO4)2、磷灰石Ca5F(PO4)3等。
(1)磷的某种核素中,中子数比质子数多1,则表示该核素的原子符号为____。
(2)磷酸钙与焦炭、石英砂混合,在电炉中加热到1500℃生成白磷,反应为:2Ca3(PO4)2+6SiO2===6CaSiO3+P4O10 10C+P4O10===P4↑+10CO↑,上述反应中的各种物质,属于酸性氧化物的有__。
(Ⅱ)(3)离子交换膜是一类具有离子交换功能的高分子材料.一容器被离子交换膜分成左右两部分,如右图所示.若该交换膜为阳离子交换膜(只允许阳离子自由通过),左边充满盐酸酸化的H2O2溶液,右边充满滴有KSCN溶液的FeCl2溶液(足量),一段时间后右边可观察到的现象:_______,若该交换膜为阴离子交换膜(只允许阴离子自由通过),左边充满含2mol NH4Al(SO4)2的溶液,右边充满含3mol Ba(OH)2的溶液,当有2mol SO42﹣通过交换膜时(若反应迅速完全),则左右两室沉淀的物质的量之比为__________________.
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:4HCl(g)+O2(g)2Cl2(g)+ 2H2O(g),该反应放出123kJ/mol的热量。其中相关的化学键键能数据如下:其中a的值为
化学键 | H—Cl | O=O | Cl—Cl | H—O |
E/(kJ/mol) | 431 | 497 | a | 465 |
A.242B.303.5C.180.5D.365
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)常温下,0.1mol/L 的CH3COOH 溶液中有1% CH3COOH 分子发生电离,则溶液的pH=______________;可以使0.10mol·L-1 CH3COOH的电离程度增大的是____________。、
a.加入少量0.10 mol·L-1的稀盐酸 b.加热CH3COOH溶液
c.加水稀释至0.010 mol·L-1. d.加入少量冰醋酸
e.加入少量氯化钠固体 f.加入少量0.10 mol·L-1的NaOH溶液
(2)将等质量的锌投入等体积且pH 均等于3 的醋酸和盐酸溶液中,经过充分反应后,发现只在一种溶液有锌粉剩余,则生成氢气的体积:V( 盐酸)________V(醋酸)(填“>”、“ <” 或“=”)。
(3)0.1mol/L 的某酸H2A 的pH=4,则H2A 的电离方程式为_________________。
(4)某温度下,Kw=1×10-12,将0.02mol/L的Ba(OH)2溶液与等物质的量浓度的NaHSO4溶液等体积混合,所得混和液的pH=____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】既能与酸(H+)反应,又能与碱(OH-)反应的化合物是( )
①MgO②Al(OH)3③NaHSO4④NaHCO3⑤CH3COONH4⑥Al
A.②④B.②③④C.②④⑤D.②④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家哈伯因为氨气的合成曾获1918年诺贝尔奖。
(1)写出实验室制取氨气的化学方程式_________。检验氨气已装满的方法是________。
(2)氨气可用如图装置进行喷泉实验,把氨气换成______(填序号)也可形成喷泉实验。
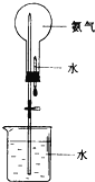
A.二氧化碳 B.氧气 C.氯化氢气体 D.氢气
(3)完成氨催化氧化生成为NO的反应方程式,4NH3+____O2===4NO+6_____,产物NO能在通常状况下被空气氧化为NO2,请完成下列反应生成硝酸的化学方程式:4NO+__O2+2H2O===4HNO3,___NO2+____O2 +__H2O===4HNO3
(4)12.8 g Cu与足量的浓硝酸反应生成的气体与一定量的O2混合,然后通入水中恰好完全反应无气体剩余,则该氧气的物质的量为_______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知有机物A、B、C、D、E、F有以下转化关系。A的产量可以衡量一个国家的石油化工发展水平;E是不溶于水且具有香味的无色液体,相对分子质量是C的2倍;F为高分子化合物。结合下图关系回答问题:
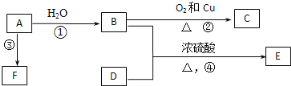
(1)写出C的结构简式:___________。
(2)写出B、D中官能团的名称:B____________,D_____________。
(3)写出下列反应的化学方程式:
②_________________________。
④________________________。
(4)物质B可以直接被氧化为D,需加入的试剂是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某温度下CH3COOH和NH3·H2O的电离常数相等,现向10 mL浓度为0.1 mol·L-1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中( )
A. 水的电离程度始终增大
B. ![]() 先增大再减小
先增大再减小
C. c(CH3COOH)与c(CH3COO-)之和始终保持不变
D. 当加入氨水的体积为10 mL时,c (NH4+)=c(CH3COO-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com