
| ||
| �� |
| ||
| �� |


 ��У��ʦ������ҵ���Ӻ����Ծ�ϵ�д�
��У��ʦ������ҵ���Ӻ����Ծ�ϵ�д� ȫ�̽��ϵ�д�
ȫ�̽��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
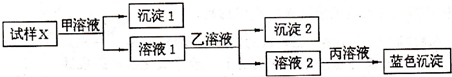
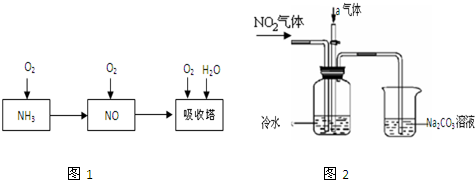
| A���٢� | B���٢� | C���ڢ� | D���ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����ͺ�ˮ��CCl4��ˮ�������ʣ������÷�Һ©�����з��� |
| B����1L 5.0mol/L HCl��Һ��ȡ����10 mL��ȡ����HCl��Һ��Ũ��Ϊ5.0 mol/L |
| C����ɢϵ���ݷ�ɢ�����Ӵ�С�ɷ�Ϊ��Һ�����塢��Һ |
| D��0.5 molCuO��Ħ������Ϊ40g/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��240 mL 0.2 mol?L-1��NaCl��Һ���ƣ���Ҫʹ����ƽ��250 mL����ƿ������ |
| B����FeCl3ϡ��Һ�еμ�NaOH��Һ����������У����Ʊ�Fe��OH��3���� |
| C��������NaOH��Һ����Ƥ���ϣ�Ӧ�����ý϶��ˮ��ϴ |
| D���ñ���ȡ��ˮ�еĵ�ʱ����ȡ����Ͳ㲻�ܴӷ�Һ©���¶˷ų� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
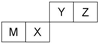
| A��X �������̬�⻯������ȶ��Ա�Z��С |
| B��Zλ��Ԫ�����ڱ��е�2���ڡ��ڢ�A�� |
| C��ԭ�Ӱ뾶Z��M |
| D��Y������������Ӧˮ��������Ա�X ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
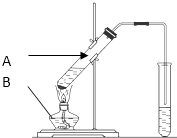 �۲����нṹ��ʽ���ش��������⣺
�۲����нṹ��ʽ���ش��������⣺
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
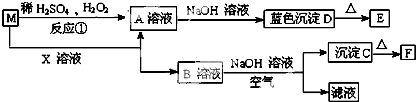
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1����H2��Cl2��Ӧ���ų�����184.6 kJ |
| B��1 mol H2��g����ȫ��Ӧ����2 mol HCl��g�����ų�������Ϊ184.6 kJ |
| C����101 kPa��25��������£�1 mol H2��g����1 mol Cl2��g����ȫ��Ӧ����2 mol HCl��g���ų�������Ϊ184.6 kJ |
| D����101 kPa��25��������£�1 mol H2��g����1 mol Cl2��g����ȫ��Ӧ����2 mol HCl��g�����յ�����Ϊ184.6 kJ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com